题目内容
15.石灰浆可用来抹墙砌砖,长期盛放石灰水的瓶子内壁常附有一层白色物质.解释以上两个问题都可用同一化学方程式,它是Ca(OH)2+CO2═CaCO3↓+H2O.分析 石灰水的溶质是氢氧化钙,氢氧化钙可以和酸性物质反应,氢氧化钙和二氧化碳生成碳酸钙沉淀和水.
解答 解:石灰水的溶质是氢氧化钙,碱可以和酸性氧化物反应生成盐和水.氢氧化钙和二氧化碳生成碳酸钙沉淀和水,书写方程式时注意配平和沉淀符号,故答案为:Ca(OH)2+CO2═CaCO3↓+H2O.
点评 掌握碱的化学性质,书写化学方程式时注意反应条件、气体符号、沉淀符号、配平等.

练习册系列答案
相关题目
15.下列现象属于化学变化的是( )
| A. | 自行车车胎受热爆炸 | B. | 铁生锈 | ||
| C. | 蜡烛融化 | D. | 海水蒸发 |
3.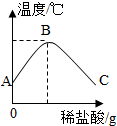 将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示,则下列说法错误的是( )
将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示,则下列说法错误的是( )
 将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示,则下列说法错误的是( )
将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示,则下列说法错误的是( )| A. | B点时,往烧杯中滴加无色酚酞试液,溶液变红色 | |
| B. | 从A到B过程中,烧杯中溶液的pH逐渐减小 | |
| C. | 稀盐酸与氢氧化钠溶液发生的反应是放热反应 | |
| D. | C点时烧杯中含有的溶质是NaCl、HCl |
10.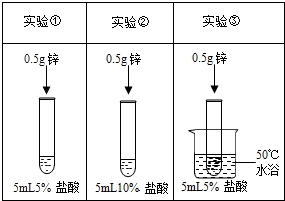 为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了如图实验.下列说法不正确的是( )
为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了如图实验.下列说法不正确的是( )
 为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了如图实验.下列说法不正确的是( )
为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了如图实验.下列说法不正确的是( )| A. | 对比实验①和②,可研究盐酸的溶质质量分数对反应剧烈程度的影响 | |
| B. | 对比实验①和③,可研究温度对反应剧烈程度的影响 | |
| C. | 对比实验②和③,可研究盐酸的溶质质量分数对反应剧烈程度的影响 | |
| D. | 此实验运用了控制变量法与对比实验法 |
20.水(H2O)被称为“生命之源”,双氧水(H2O2)被称为“绿色氧化剂”.下列关于它们的说法中正确的是( )
| A. | 分子构成相同 | B. | 组成元素的种类相同 | ||
| C. | 都含有氢分子 | D. | 性质相似 |
7.元素周期表是学习和研究化学的重要工具.请根据如表(元素周期表的部分内容)回答有关问题:
(1)查出空气中含量最多元素的相对原子质量为14.01;
(2)在元素周期表中,同一周期中(横行)的元素,除0族(最右纵行)元素外,从左到右原子序数依次增大,原子半径逐渐减少.则原子半径:钠>镁(填“>”或“<”或“=”);
(3)第3周期第ⅥA元素的原子得到2个电子后形成了离子,该离子符号是S2-.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(2)在元素周期表中,同一周期中(横行)的元素,除0族(最右纵行)元素外,从左到右原子序数依次增大,原子半径逐渐减少.则原子半径:钠>镁(填“>”或“<”或“=”);
(3)第3周期第ⅥA元素的原子得到2个电子后形成了离子,该离子符号是S2-.
4.已知反应A+B=C+D且A与B参加反应的质量比为4:3,若反应后生成C和D的质量共为2.8g,则消耗的反应物B为( )
| A. | 0.3g | B. | 0.9g | C. | 1.2 g | D. | 1.6 g |
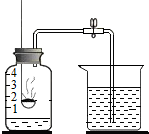 化学兴趣小组用如图所示装置测定空气中氧气的含量
化学兴趣小组用如图所示装置测定空气中氧气的含量