题目内容
14.某溶液中含有Na+、H+、Cl-、SO42-四种离子:(1)若在溶液中加入紫色石蕊试液,显红色,说明溶液pH<7;
(2)溶液中存在的酸可能是盐酸或硫酸 (写物质名称,写成化学式不得分)
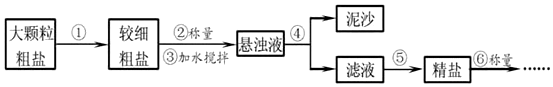
(3)若要除去溶液中的SO42-而不引入其他种类的离子,应该加入适量的试剂是氯化钡;然后进行的实验操作是B (填字母)
A.溶解 B.过滤 C.结晶.
分析 (1)依据指示剂与pH的关系分析.
(2)溶液中存在的阴离子是判断酸的种类.
(3)利用硫酸根遇钡离子会生成白色沉淀分析判断.
(4)溶液中的硫酸根转化成硫酸钡沉淀后,可用过滤的方法分析判断.
解答 解:(1)溶液中滴入紫色石蕊溶液显红色说明溶液显酸性,pH小于7.
(2)从溶液中存在的阴离子是Cl-、SO42-与氢结合会是盐酸或硫酸.
(3)硫酸根遇钡离子会生成白色沉淀为不引入新的杂质离子所以应该加入氯化钡溶液.
(4)溶液中的硫酸根遇钡会转化成硫酸钡沉淀,把沉淀去除的方式是过滤.
故答案为:(1)<;(2)盐酸;硫酸;(3)氯化钡;B.
点评 本题考查了常见离子的性质及检验,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
4.下列有关物质制备的药品及原理完全正确的是( )
| A. | 实验室制二氧化碳:CaCO3+H2SO4=CaSO4+H2O+CO2↑ | |
| B. | 实验室制氧气:H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2↑+O2↑ | |
| C. | 实验室制氢气:Zn+2HCl=ZnCl2+H2↑ | |
| D. | 实验室模拟炼铁:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 |
19.某兴趣小组的同学对一批含铜的铁样品进行分析,甲、乙、丙三位同学分别进行实验,其中一位同学所用的稀硫酸与铁样品恰好完全反应,实验数据如表:
请你认真分析数据,回答下列问题:
(1)乙同学所用的稀硫酸与铁的样品恰好完全反应?
(2)计算铁的样品中铁的质量分数.
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸的质量(克) | 200 | 150 | 150 |
| 加入铁的样品的质量(克) | 8 | 8 | 14 |
| 充分反应后,烧杯+剩余物的质量(克) | 207.8 | 157.8 | 163.8 |
(1)乙同学所用的稀硫酸与铁的样品恰好完全反应?
(2)计算铁的样品中铁的质量分数.
6.今年春季我国出现H7N9禽流感疫情,帕拉米韦是一种治疗H7N9禽流感的新药,其化学式是H15H28N4O4,有关该物质的下列说法不正确的是( )
| A. | 帕拉米韦属于有机化合物 | |
| B. | 帕拉米韦由碳、氢、氮、氧四种元素组成 | |
| C. | 一个分子中含有51个原子 | |
| D. | 帕拉米韦中氢元素质量分数最大 |
4.人体呼出气体的各成分的含量数据测定如下,其中最不可能的是( )
| A. | 氮气 76% | B. | 氧气 22% | C. | 二氧化碳 4% | D. | 水蒸气 14% |
 a、b、c三种固体物质(均不含结晶水)在水中的溶解度曲线如图所示.
a、b、c三种固体物质(均不含结晶水)在水中的溶解度曲线如图所示.