题目内容
9.氯化钠是生活必需品,也是重要的化工原料.提纯含少量泥沙的粗盐,一般经过以下操作流程: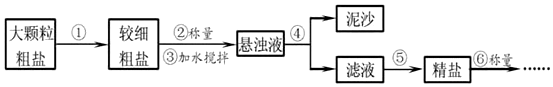
(1)操作④中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是D.
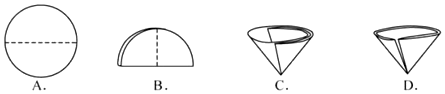
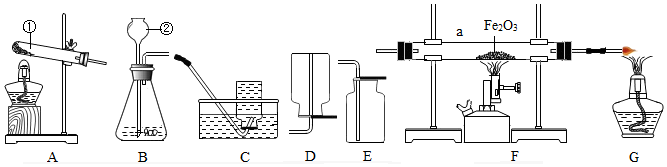
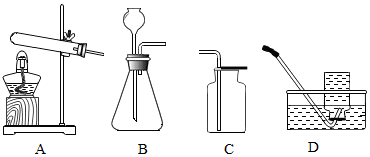
(2)进行④操作时,下列做法错误的是D.
A.玻璃棒要靠在三层滤纸的一边 B.漏斗下端的管口要紧靠烧杯的内壁
C.滤纸的边缘要低于漏斗口 D.滤纸边缘低于液面
(3)向滤液中加入活性炭,利用其吸附性,除去水样中的色素和异味.
(4)实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较低,其可能原因是ABD.
A.食盐没有全部溶解即过滤 B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿 D.器皿上沾有的精盐没全部转移到称量纸上.
分析 (1)根据制作过滤器的操作过程分析判断;
(2)根据过滤操作的注意事项分析判断;
(3)根据活性炭的作用进行分析判断;
(4)可以根据质量分数的比例式进行分析,精盐的质量少了或者粗盐的质量大了.
解答 解:(1)A、B、C 是滤纸的正确的折叠方法,D中的滤纸,接口处出现缝隙,液体会直接的进入下面的烧杯,故不该出现的情形是D;故填:D;
(2)操作④是将固体和液体分离,因此是过滤.
A.过滤时玻璃棒要靠在三层滤纸的一边,故说法正确;
B.漏斗下端的管口要紧靠烧杯的内壁,以防液体溅出,故说法正确;
C.滤纸的边缘要低于漏斗口,故说法正确;
D.滤纸边缘要高于液面,以防过滤后仍浑浊,故说法错误.
故选D;
(3)向滤液中加入活性炭,利用其吸附性,除去水样中的色素和异味,故填:吸附;
(4)既然粗盐的产率低说明在提纯时,损失了精盐,
A、食盐没有完全溶解,会使精盐的质量减少,故A正确,
B、食盐飞溅了导致了精盐的减少,故B正确,
C、精盐很潮增大了精盐的质量,会使质量分数增大,故C错误,
D、蒸发皿中的精盐没有全部转移到称量纸上,会使精盐的质量减小,故D正确,
故选:ABD.
点评 本题主要对粗盐提纯的实验中涉及的知识进行了全面的考查,要理论联系实际.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
20.归纳是一种重要的学习方法.下列归纳中错误的是( )
| A. | 酸都能与盐发生复分解反应 | B. | 氧化物都只有两种元素 | ||
| C. | 所有化学变化都遵守质量守恒定律 | D. | 物质与氧气的反应都属于氧化反应 |
4.分析处理图表中的信息是学习科学的一种重要方法.如表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
(1)40℃时,氯化钠的溶解度为36.6克.
(2)碳酸钠的溶解度随温度的升高而增大(填“增大”或“减小”),在20℃时,将30克碳酸钠加入100克水中,充分搅拌后得到的是饱和溶液(填“饱和溶液”或“不饱和溶液”),将上述溶液升温到30℃,该溶液的溶质质量分数为23.1%(结果精确到0.1%).
(3)10℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的溶液是碳酸钠饱和溶液.
| 温度/℃ | 10 | 20 | 30 | 40 |
| 氯化钠溶解度/克 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸钠溶解度/克 | 12.2 | 21.8 | 39.7 | 53.2 |
(2)碳酸钠的溶解度随温度的升高而增大(填“增大”或“减小”),在20℃时,将30克碳酸钠加入100克水中,充分搅拌后得到的是饱和溶液(填“饱和溶液”或“不饱和溶液”),将上述溶液升温到30℃,该溶液的溶质质量分数为23.1%(结果精确到0.1%).
(3)10℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的溶液是碳酸钠饱和溶液.
18.由A、B两种元素组成的化合物中A、B的质量比为3:1,A与B的相对原子质量比为12:1,则该化合物化学式为( )
| A. | AB | B. | AB2 | C. | AB4 | D. | A2B |
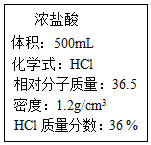 某浓盐酸瓶上的标签如图所示.求:
某浓盐酸瓶上的标签如图所示.求: