题目内容
18. 实验室有一瓶氢氧化钠溶液,瓶上标签内容如图所示,请你根据标签上提供的数据解答下列问题:
实验室有一瓶氢氧化钠溶液,瓶上标签内容如图所示,请你根据标签上提供的数据解答下列问题:(1)用20g该氢氧化钠溶液可以配制质量分数为10%的氢氧化钠溶液多少克?
(2)利用刚配制好的氢氧化钠与100g稀盐酸,当加入到40g时,恰好完全中和,求稀盐酸中溶质的质量分数.
分析 (1)根据稀释前后溶质的质量不变分析;
(2)根据氢氧化钠的质量结合方程式计算氯化氢的质量,进一步计算稀盐酸中溶质的质量分数.
解答 解:(1)设可以配制10%的氢氧化钠溶液的质量为X
20g×50%═X×10%
X=100g
(2)设盐酸中溶质质量为Y
HCl+NaOH═NaCl+H2O
36.5 40
Y 40g×10%
$\frac{36.5}{Y}=\frac{40}{40g×10%}$
Y=3.65g
稀盐酸中溶质质量分数=$\frac{36.5g}{100g}$×100%═3.65%
答:稀盐酸中溶质质量分数为3.65%.
点评 本题主要考查学生运用溶液稀释前后溶质的质量不变和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.某化学兴趣小组为测定某有机物(含C、H、O三种元素)中各元素的质量比,用如图实验装置(部分夹持装置略去)进行探究.
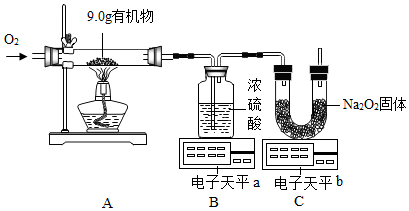
提示:装置C中发生的反应为2Na2O2+2CO2=2Na2CO3+O2
实验数据:
请计算该有机物中各元素的质量比(写出计算过程).

提示:装置C中发生的反应为2Na2O2+2CO2=2Na2CO3+O2
实验数据:
| 读数 | 反应前质量/g | 反应后质量/g |
| 电子天平a | 217.0 | 222.4 |
| 电子天平b | 150.0 | 158.4 |
6.下列生产和生活中,没有用熟石灰的是( )
| A. | 农业上,改良酸性土壤 | B. | 建筑业上,粉刷墙壁 | ||
| C. | 实验室中,干燥气体 | D. | 工业上,处理硫酸厂的污水 |
13. 如图是固体物质a、b、c的溶解度曲线.下列说法正确的是( )
如图是固体物质a、b、c的溶解度曲线.下列说法正确的是( )
 如图是固体物质a、b、c的溶解度曲线.下列说法正确的是( )
如图是固体物质a、b、c的溶解度曲线.下列说法正确的是( )| A. | t1℃时,a、b、c溶解度的大小顺序是:a>b>c | |
| B. | t2℃时,a、b饱和溶液中溶质质量分数相等 | |
| C. | t2℃时,将40g 的c加到100g水中,制得的溶液不饱和 | |
| D. | 欲使c从溶液中结晶,可以采用降温结晶或蒸发溶剂的方法 |
8.下列各组离子在水中一定能大量共存,并形成无色透明溶液的是( )
| A. | Ba2+、Cu2+、SO42-、H+ | B. | H+、Ca2+、CO32-、Mg+ | ||
| C. | Fe2+、Cl-、NO3-、K+ | D. | Na+、OH-、Cl-、Ba2+ |
 (A、B、C、D为初中化学常见的四种物质,它们之间有如图所示的转化和反应关系(“→”表示某一种物质经一步反应可转化为另一种物质,“-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去)
(A、B、C、D为初中化学常见的四种物质,它们之间有如图所示的转化和反应关系(“→”表示某一种物质经一步反应可转化为另一种物质,“-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去) 如图是某反应的微观示意图.反应前后化合价没有发生变化的元素为H;该反应的化学方程式4NH3+5O2$\frac{\underline{\;一定条件\;}}{\;}$4NO+6H2O.
如图是某反应的微观示意图.反应前后化合价没有发生变化的元素为H;该反应的化学方程式4NH3+5O2$\frac{\underline{\;一定条件\;}}{\;}$4NO+6H2O.