题目内容
12.碳酸钠溶液和氯化钙溶液发生反应的化学方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl.请判断下列说法中错误的是( )| A. | 该反应属于复分解反应 | B. | 反应前后溶液的pH值降低 | ||
| C. | 反应前后,溶液的总质量保持不变 | D. | 反应能进行,是因为有沉淀生成 |
分析 A、复分解反应是两种化合物相互交换成分生成两种新的化合物的反应.
B、根据碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钠溶液显碱性,氯化钠溶液显中性,进行分析判断.
C、根据碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,进行分析判断.
D、根据复分解反应发生的条件,进行分析判断.
解答 解:A、该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,故选项说法正确.
B、碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钠溶液显碱性,氯化钠溶液显中性,反应前后溶液的pH值降低,故选项说法正确.
C、碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,由质量守恒定律,由于有沉淀生成,则反应前后,溶液的总质量减少,故选项说法错误.
D、由复分解反应发生的条件,若两种物质相互交换成分有沉淀、气体或水生成,则能发生化学反应,该反应能进行,是因为有沉淀生成,故选项说法正确.
故选:C.
点评 本题难度不大,掌握盐的化学性质、质量守恒定律、复分解反应的特征与条件是正确解答本题的关键.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
20.现有X、铜、镉(Cd)三种金属,把X和镉分别放入硫酸铜溶液中,过一会儿,发现镉表面有一层红色物质析出,而X表面没有变化,则X、铜、镉的金属活性顺序为( )
| A. | 镉>铜>X | B. | 铜>镉>X | C. | X>铜>镉 | D. | 镉>X>铜 |
17.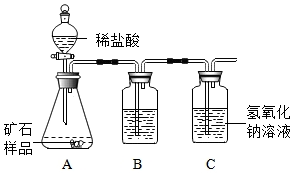 为了测定某石灰石样品中碳酸钙的质量分数(样品中所含杂质不溶于水,也不与酸反应),某同学采用如下实验装置来研究.
为了测定某石灰石样品中碳酸钙的质量分数(样品中所含杂质不溶于水,也不与酸反应),某同学采用如下实验装置来研究.
(1)装置B用来干燥气体,B中所盛的试剂可以是浓硫酸.
(2)利用如同装置进行实验时,下列情况会使碳酸钙质量分数的测量结果偏小的有③④.
①实验开始时A、B装置以及导气管内残留有少量空气
②进入C装置的气体中还混有少量HCl气体
③气体通过C装置速度过快,CO2来不及被NaOH溶液全部吸收
④实验结束时,各装置内还残留有少量CO2气体
(3)实验中取5克矿石样品,将20克稀盐酸平均分成4次注入,测量并记录每次充分反应后装置C的质量(如表),求出该矿石样品中碳酸钙的质量分数.(碳酸钙与盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑)
 为了测定某石灰石样品中碳酸钙的质量分数(样品中所含杂质不溶于水,也不与酸反应),某同学采用如下实验装置来研究.
为了测定某石灰石样品中碳酸钙的质量分数(样品中所含杂质不溶于水,也不与酸反应),某同学采用如下实验装置来研究.(1)装置B用来干燥气体,B中所盛的试剂可以是浓硫酸.
(2)利用如同装置进行实验时,下列情况会使碳酸钙质量分数的测量结果偏小的有③④.
①实验开始时A、B装置以及导气管内残留有少量空气
②进入C装置的气体中还混有少量HCl气体
③气体通过C装置速度过快,CO2来不及被NaOH溶液全部吸收
④实验结束时,各装置内还残留有少量CO2气体
(3)实验中取5克矿石样品,将20克稀盐酸平均分成4次注入,测量并记录每次充分反应后装置C的质量(如表),求出该矿石样品中碳酸钙的质量分数.(碳酸钙与盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑)
| 死眼次数 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量/克 | 5 | 5 | 5 | 5 |
| 充分反应后装置C的质量/克 | 150.52 | 151.04 | 151.56 | 151.76 |
1. 在高温条件下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小莉很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
在高温条件下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小莉很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近飘到空中的肥皂泡,有爆鸣声.说明生成的气体是 .
(3)探究试管中剩余固体成分是什么?
【查阅资料】(1)常见铁的氧化物的物理性质如下表:
(2)稀盐酸(或稀硫酸)与铁反应产生气体,与铁的氧化物反应没有气体产生.
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe3O4;
猜想二:剩余固体是Fe和Fe3O4.
【实验探究】根据猜想与假设,设计实验方案加以检验.
【实验结论】铁和水蒸气反应的化学方程式为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2↑.
【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3红棕色粉末且不能被磁铁吸引.
 在高温条件下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小莉很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
在高温条件下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小莉很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近飘到空中的肥皂泡,有爆鸣声.说明生成的气体是 .
(3)探究试管中剩余固体成分是什么?
【查阅资料】(1)常见铁的氧化物的物理性质如下表:
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe3O4;
猜想二:剩余固体是Fe和Fe3O4.
【实验探究】根据猜想与假设,设计实验方案加以检验.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量黑色固体于试管中,加入足量的稀盐酸 | 若固体全部溶解,没有气泡冒出 | 剩余固体是Fe3O4 |
【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3红棕色粉末且不能被磁铁吸引.
 一烧杯中盛有200克BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系如图所示:请根据题意回答问题:
一烧杯中盛有200克BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系如图所示:请根据题意回答问题: 利用图线能形象直观地描述科学现象,已知某固体由MgCl2和NaOH组成,取少量该固体于烧杯中向烧杯中加入足量水搅拌后,观察到由白色不溶物存在,再向烧杯中滴加稀盐酸,不溶物质量与滴加稀盐酸质量关系如图所示,请解释曲线变化的原因.
利用图线能形象直观地描述科学现象,已知某固体由MgCl2和NaOH组成,取少量该固体于烧杯中向烧杯中加入足量水搅拌后,观察到由白色不溶物存在,再向烧杯中滴加稀盐酸,不溶物质量与滴加稀盐酸质量关系如图所示,请解释曲线变化的原因.