题目内容
7. 利用图线能形象直观地描述科学现象,已知某固体由MgCl2和NaOH组成,取少量该固体于烧杯中向烧杯中加入足量水搅拌后,观察到由白色不溶物存在,再向烧杯中滴加稀盐酸,不溶物质量与滴加稀盐酸质量关系如图所示,请解释曲线变化的原因.
利用图线能形象直观地描述科学现象,已知某固体由MgCl2和NaOH组成,取少量该固体于烧杯中向烧杯中加入足量水搅拌后,观察到由白色不溶物存在,再向烧杯中滴加稀盐酸,不溶物质量与滴加稀盐酸质量关系如图所示,请解释曲线变化的原因.
分析 由于MgCl2+2NaOH=Mg(OH)2↓+2NaCl,所以白色不溶物为氢氧化镁,氢氧化镁可以溶于酸,再根据图象,加入盐酸后开始沉淀不消失,就可以完成此题的解答.
解答 解:由于MgCl2+2NaOH=Mg(OH)2↓+2NaCl,所以白色不溶物为氢氧化镁,氢氧化镁可以溶于酸,由于图象中最初沉淀没有变化,说明盐酸与另外的物质反应,说明氢氧化钠过量,滴加的盐酸先和过量的氢氧化钠反应,所以开始阶段沉淀质量不变,后来盐酸与氢氧化镁反应生成氯化镁和水,使沉淀逐渐减少直到沉淀完全消失.
故答案为:由于MgCl2+2NaOH=Mg(OH)2↓+2NaCl,所以白色不溶物为氢氧化镁,氢氧化钠过量,滴加的盐酸先和过量的氢氧化钠反应,所以开始阶段沉淀质量不变,后来盐酸与氢氧化镁反应生成氯化镁和水,使沉淀逐渐减少直到沉淀完全消失.
点评 本题结合图象,考查了常见的酸碱盐之间的复分解反应以及有关的实验现象.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.酸与碱作用生成盐和水的反应,叫做中和反应,它在工农业生产和日常生活中有着广泛的用途,下列不属于中和反应应用的是( )
| A. | 用稀硫酸除铁锈 | |
| B. | 施用熟石灰改良酸性土壤 | |
| C. | 用氢氧化钠溶液洗涤石油产品中残余的硫酸 | |
| D. | 服用含氢氧化铝的药物(如斯达舒)来治疗胃酸过多 |
12.碳酸钠溶液和氯化钙溶液发生反应的化学方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl.请判断下列说法中错误的是( )
| A. | 该反应属于复分解反应 | B. | 反应前后溶液的pH值降低 | ||
| C. | 反应前后,溶液的总质量保持不变 | D. | 反应能进行,是因为有沉淀生成 |
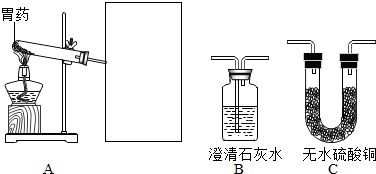
17.(1)某化学兴趣小组利用如图装置探究制取气体的原理、方法.结合装置图,回答下列问题:

①写出图中标号仪器的名称:a长颈漏斗,b锥形瓶.
②用高锰酸钾制取氧气时,可选用的发生装置是A (填如图字母),可选用C装置收集氧气,其原因是氧气的密度比空气大,实验时应在试管口放一团棉花,其作用是防止加热时高锰酸钾粉末进入导管,用排水法收集氧气的合适时间是导管口气泡连续、均匀冒出时,写出该反应的表达式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.其反应类型为分解反应.
③实验室常用氯化铵固体与碱石灰固体共热来制取一种易溶于水密度比空气小的氨气(NH3),应选择的制取装置是A、D (填上图字母).
(2)【发现问题】:小明同学用“双氧水”(过氧化氢溶液)清洗伤口时,不小心将过氧化氢溶液滴到水泥板上,发现大量气泡产生.
①【提出问题】:小明联想到自己曾经用二氧化锰作过氧化氢的催化剂,他想,水泥块能否作过氧化氢分解的催化剂呢?于是他到建筑工地取回一些小水泥块,并用蒸馏水浸泡、冲洗、干燥,并进行以下探究.
②【猜想】:水泥块能作过氧化氢分解的催化剂.
③【实验验证】:
④【结论】:水泥块能加快过氧化氢的分解速率,故水泥块是过氧化氢分解的催化剂.
⑤【讨论与反思】:小冰认为:仅凭上述两个实验还不能证明水泥块为过氧化氢分解的催化剂,他觉得需要增加一个探究实验:称量反应前后水泥块的质量是否改变;
实验步骤:Ⅰ准确称量水泥块质量;Ⅱ完成实验二;Ⅲ待反应结束,将实验二试管里的物质进行过滤、洗涤、干燥、称量;Ⅳ对比反应前后水泥块的质量;
⑥但老师指出:要证明小明的猜想,小冰的补充实验还是不足够,需要再补充一个探究实验:在装有过氧化氢溶液的试管中加入实验二中的水泥块,然后用带火星木条伸入,观察是否复燃.

①写出图中标号仪器的名称:a长颈漏斗,b锥形瓶.
②用高锰酸钾制取氧气时,可选用的发生装置是A (填如图字母),可选用C装置收集氧气,其原因是氧气的密度比空气大,实验时应在试管口放一团棉花,其作用是防止加热时高锰酸钾粉末进入导管,用排水法收集氧气的合适时间是导管口气泡连续、均匀冒出时,写出该反应的表达式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.其反应类型为分解反应.
③实验室常用氯化铵固体与碱石灰固体共热来制取一种易溶于水密度比空气小的氨气(NH3),应选择的制取装置是A、D (填上图字母).
(2)【发现问题】:小明同学用“双氧水”(过氧化氢溶液)清洗伤口时,不小心将过氧化氢溶液滴到水泥板上,发现大量气泡产生.
①【提出问题】:小明联想到自己曾经用二氧化锰作过氧化氢的催化剂,他想,水泥块能否作过氧化氢分解的催化剂呢?于是他到建筑工地取回一些小水泥块,并用蒸馏水浸泡、冲洗、干燥,并进行以下探究.
②【猜想】:水泥块能作过氧化氢分解的催化剂.
③【实验验证】:
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 将带火星的木条伸入装有过氧化氢溶液的试管中. | 木条不复燃 | 常温下过氧化氢溶液分解很慢. |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 | 木条复燃 | 加入水泥块能加快过氧化氢溶液的分解速率 |
⑤【讨论与反思】:小冰认为:仅凭上述两个实验还不能证明水泥块为过氧化氢分解的催化剂,他觉得需要增加一个探究实验:称量反应前后水泥块的质量是否改变;
实验步骤:Ⅰ准确称量水泥块质量;Ⅱ完成实验二;Ⅲ待反应结束,将实验二试管里的物质进行过滤、洗涤、干燥、称量;Ⅳ对比反应前后水泥块的质量;
⑥但老师指出:要证明小明的猜想,小冰的补充实验还是不足够,需要再补充一个探究实验:在装有过氧化氢溶液的试管中加入实验二中的水泥块,然后用带火星木条伸入,观察是否复燃.