题目内容
17.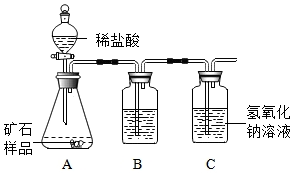 为了测定某石灰石样品中碳酸钙的质量分数(样品中所含杂质不溶于水,也不与酸反应),某同学采用如下实验装置来研究.
为了测定某石灰石样品中碳酸钙的质量分数(样品中所含杂质不溶于水,也不与酸反应),某同学采用如下实验装置来研究.(1)装置B用来干燥气体,B中所盛的试剂可以是浓硫酸.
(2)利用如同装置进行实验时,下列情况会使碳酸钙质量分数的测量结果偏小的有③④.
①实验开始时A、B装置以及导气管内残留有少量空气
②进入C装置的气体中还混有少量HCl气体
③气体通过C装置速度过快,CO2来不及被NaOH溶液全部吸收
④实验结束时,各装置内还残留有少量CO2气体
(3)实验中取5克矿石样品,将20克稀盐酸平均分成4次注入,测量并记录每次充分反应后装置C的质量(如表),求出该矿石样品中碳酸钙的质量分数.(碳酸钙与盐酸反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑)
| 死眼次数 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量/克 | 5 | 5 | 5 | 5 |
| 充分反应后装置C的质量/克 | 150.52 | 151.04 | 151.56 | 151.76 |
分析 (1)二氧化碳气体可用浓硫酸来干燥;
(2)根据装置的特点和实验的过程分析对计算出碳酸钙质量的影响;
(3)根据质量守恒定律C装置的质量增加量为吸收的二氧化碳的质量,根据二氧化碳的质量可计算出碳酸钙的质量即可计算出矿石样品中碳酸钙的质量分数.
解答 解:(1)装置B用来干燥气体,B中所盛的试剂可以是浓硫酸.
(2)①实验开始时A、B装置以及导气管内残留有少量空气,对计算碳酸钙的质量不影响;
②进入C装置的气体中还混有少量HCl气体,HCl气体能与氢氧化钠溶液反应,使计算出碳酸钙的质量偏大,测量结果偏大;
③气体通过C装置速度过快,CO2来不及被NaOH溶液全部吸收,使计算出碳酸钙的质量偏小,测量结果偏小;
④实验结束时,各装置内还残留有少量CO2气体,使计算出碳酸钙的质量偏小,测量结果偏小.
(3)A装置是气体发生装置,B装置是气体干燥装置,C、装置是二氧化碳收集装置.所以C装置的质量增加量为吸收的二氧化碳的质量将数据加工如下:
| 实验次数 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量/克 | 5 | 5 | 5 | 5 |
| C装置的起始质量/克 | 150 | 150.52 | 151.04 | 151.56 |
| 充分反应后装置C的质量/克 | 150.52 | 151.04 | 151.56 | 151.76 |
| C装置的质量变化/克 | 推出0.52 | 0.52 | 0.52 | 0.2 |
设生成1.76g二氧化碳需要的碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 1.76g
$\frac{100}{44}=\frac{x}{1.76g}$ 解得:x=4g
则石灰石样品中碳酸钙的质量分数为:$\frac{4g}{5g}$×100%=80%
故答为:(1)浓硫酸;(2)③④;(3)石灰石样品中碳酸钙的质量分数为80%
点评 明确实验设计原理,根据原理分析实验装置的作用,进而根据给出的数据计算.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
7.分别将下列物质同时加入水中,能共存且形成无色透明溶液的是( )
| A. | 碳酸钠、氯化钾、硫酸钠 | B. | 硫酸铜、盐酸、氯化钾 | ||
| C. | 盐酸、氢氧化钾、碳酸钠 | D. | 硝酸银、氯化钡、硝酸 |
8.钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图甲所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如图2.请根据有关信息回答问题.
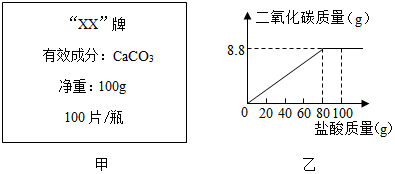
(1)如何判断钙片中的碳酸钙已经反应完当加入过量的盐酸,不再有气泡冒出.
(2)a的数值为25.
(3)该品牌补钙药剂中CaCO3的质量分数是多少?
(4)求该盐酸中溶质的质量分数为(写出计算过程,计算结果保留一位小数)

| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 | 20 |
| 剩余固体的质量(g) | 35 | 30 | a | 20 |
(2)a的数值为25.
(3)该品牌补钙药剂中CaCO3的质量分数是多少?
(4)求该盐酸中溶质的质量分数为(写出计算过程,计算结果保留一位小数)
12.碳酸钠溶液和氯化钙溶液发生反应的化学方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl.请判断下列说法中错误的是( )
| A. | 该反应属于复分解反应 | B. | 反应前后溶液的pH值降低 | ||
| C. | 反应前后,溶液的总质量保持不变 | D. | 反应能进行,是因为有沉淀生成 |
2.下列实验操作能达到预期目的是( )
| A. | 将混合气体导出并点燃,来除去CO2中混有的少量CO | |
| B. | 将酚酞试液滴入Cu(OH)2中,通过酚酞颜色的变化判断Cu(OH)2是否属于碱 | |
| C. | 将50g溶质质量分数为10%的盐酸加热蒸发25g水,得到质量分数为20%的盐酸 | |
| D. | 按溶解、过滤、蒸发、干燥的操作顺序可以分力氯化钙、碳酸钙 |
7.我们身边的下列物质中,属于纯净物的是( )
| A. | 冰镇啤酒 | B. | 新鲜空气 | C. | 酱油 | D. | 冰水 |