题目内容
1.某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究:
【查阅资料】
| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
(1)探究两者水溶液酸碱性的差异
| 实验步骤 | 实验现象 | 实验结论 |
| ①分别向等浓度、等体积的纯碱溶液和小苏打溶液中滴加2滴酚酞溶液 | 溶液均变红色,且纯碱溶液中颜色更深 | 两种溶液均呈碱性,且纯碱溶液的碱性更强 |
| ②用玻璃棒分别蘸取两种溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较 | 纯碱溶液的pH=11,小苏打溶液的pH=9 |
该小组按如图所示装置进行实验操作,观察到乙(选填“甲”或“乙”)烧杯中澄清石灰水变浑浊,相应的试管中发生反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
【反思评价】有同学认为如图装置不够严密,理由是试管口需要放一团棉花.
分析 根据表中关于碳酸钠和碳酸氢钠的酸碱性及热稳定性所提供的信息分析解答;根据反应物和生成物,正确书写化学方程式.
解答 解:(1)从表中可以看出食用纯碱和食用小苏打的水溶液均显碱性,遇酚酞均能使酚酞变红,且碱性越强颜色越红,测定溶液酸碱性强弱程度可采用pH试纸测定,要把颜色与标准比色卡对比;
(2)由图表关于两者的热稳定性进行分析可知:食用小苏打可以加热分解生成二氧化碳,而食用纯碱不能,所以分析装置可知乙烧杯的澄清石灰水变浑浊,其分解的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;
【反思评价】碳酸钠、碳酸氢钠属于粉末状,加热时,可能堵塞导管,需要在试管口放一团棉花.
故答案为:(1)
| 实验步骤 | 实验现象 | 实验结论 |
| ①分别向等浓度、等体积的纯碱溶液和小苏打溶液中滴加2滴酚酞溶液 | 溶液均变红色,且纯碱溶液中颜色更深 | 两种溶液均呈碱性,且纯碱溶液的碱性更强 |
| ②用玻璃棒分别蘸取两种溶液滴到pH试纸上,把试纸显示的颜色与 标准比色卡比较 | 纯碱溶液的pH=11,小苏打溶液的pH=9 |
【反思评价】试管口需要放一团棉花.
点评 此题是一道实验探究题,解题的关键是利用相关题目中的信息结合探究过程中有关的反应进行分析判断,题目难度不大,注重基础,能较好的训练和强化学生所学的基础知识.

练习册系列答案
相关题目
10.日常生活中发生的下列变化属于化学变化的是( )
| A. | 玻璃破碎 | B. | 木材制成桌椅 | C. | 菜刀生锈 | D. | 湿衣服晾干 |

 如图所示为元素周期表的一部分,已知D元素的原子核内有16个质子,请回答下列问题:
如图所示为元素周期表的一部分,已知D元素的原子核内有16个质子,请回答下列问题: 小芳用软塑料瓶自制气体发生装置,通过捏放瓶身可随时控制反应发生和停止(如图).若利用该装置制二氧化碳,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.若利用该装置制氧气,无纺布包内药品为二氧化锰.
小芳用软塑料瓶自制气体发生装置,通过捏放瓶身可随时控制反应发生和停止(如图).若利用该装置制二氧化碳,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.若利用该装置制氧气,无纺布包内药品为二氧化锰.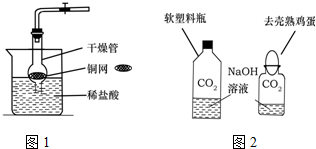 CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质:
CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质: