题目内容
14.现有HCl与CaCl2的混合溶液,为了分析混合溶液中HCl和CaCl2的质量分数,设计了如下实验方案:
实验中混合溶液与Na2CO3溶液恰好完全反应,实验共记录了两组数据:
第①组,气体吸收完全后,NaOH溶液质量增加4.4g;
第②组,沉淀完全后,经过滤、洗涤、烘干后得到固体的质量为10g.根据实验设计及有关数据进行分析与计算:
(1)混合溶液中HCl的质量分数为7.3%.(只写结果)
(2)混合溶液中CaCl2的质量分数为多少?(写出计算过程)
分析 稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,氯化钙和碳酸钠反应生成白色沉淀碳酸钙和氯化钠;
氢氧化钠溶液增加的质量即为反应生成二氧化碳的质量,经过滤、洗涤、烘干后得到固体的质量即为反应生成碳酸钙的质量,根据提供的数据可以进行相关方面的计算.
解答 解:(1)设氯化氢的质量为x,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
73 44
x 4.4g
$\frac{73}{x}$=$\frac{44}{4.4g}$,
x=7.3g,
混合溶液中HCl的质量分数为:$\frac{7.3g}{100g}$×100%=7.3%,
故填:7.3%.
(2)设氯化钙的质量维护y,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
111 100
y 10g
$\frac{111}{y}$=$\frac{100}{10g}$,
y=11.1g,
氯化钙的质量分数为:$\frac{11.1g}{100g}$×100%=11.1%,
答:氯化钙的质量分数是11.1%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
11.下列调味品加入适量水后不能形成溶液的是( )
| A. | 食用油 | B. | 食盐 | C. | 味精 | D. | 蔗糖 |
5.世界上每年因锈蚀而报废的金属设备和材料,高达产量的20%~40%.某实验小组对铁的燃烧和锈蚀进行如下探究.

探究一:铁丝燃烧
如图1所示,取3根粗细、长度均相同的光亮细铁丝,将其中两根分别盘成螺旋状,在每根铁丝一端系上粗铜丝,另一端系一根火柴杆,点燃火柴杆,待快燃尽时,分别插入充满氧气的集气瓶中.观察到:Ⅰ、Ⅱ中铁丝都剧烈燃烧,且Ⅱ中铁丝燃烧比Ⅰ中的更剧烈;Ⅲ中铁丝没有燃烧.
(1)集气瓶中加入少量水的作用:防止高温熔化物溅落炸裂瓶底.
(2)为什么Ⅲ中铁丝不能燃烧?实验III中火柴在铁丝上方,用其火焰内焰对铁丝加热,内焰温度低,没有对铁丝充分预热,因此不能达到铁丝的着火点.
(3)分析Ⅱ中铁丝燃烧比Ⅰ中更剧烈的原因:实验II中铁丝绕成螺旋状,与氧气接触面积增大,反应更充分.
探究二:铁粉腐蚀的条件
如图2所示,将所有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,观察到量筒内水沿着细导管慢慢进入广口瓶(容积为146mL).当温度恢复至室温,量筒内水面高度不变时读数(此时广口瓶内氧气含量几乎为零),记录量筒的起始和最终读数以及所需时间如下表:
(1)实验①和②说明NaCl可以加快(选填“加快”或“减慢”)铁锈蚀的过程.
(2)实验开始后,广口瓶温度上升,说明铁锈蚀是放热(选填“放热”或“吸热”)过程.
(3)实验①和③是探究炭粉对铁锈蚀速率的影响,实验③表格空白处样品的组成是1g铁粉和10滴水.
(4)该装置还可用于测量空气中氧气的含量,根据上述数据计算得出空气中氧气的体积分数约是19.2%(精确到百分号前小数点后一位),试分析该实验结果出现误差的原因:滤纸包占有一定体积.

探究一:铁丝燃烧
如图1所示,取3根粗细、长度均相同的光亮细铁丝,将其中两根分别盘成螺旋状,在每根铁丝一端系上粗铜丝,另一端系一根火柴杆,点燃火柴杆,待快燃尽时,分别插入充满氧气的集气瓶中.观察到:Ⅰ、Ⅱ中铁丝都剧烈燃烧,且Ⅱ中铁丝燃烧比Ⅰ中的更剧烈;Ⅲ中铁丝没有燃烧.
(1)集气瓶中加入少量水的作用:防止高温熔化物溅落炸裂瓶底.
(2)为什么Ⅲ中铁丝不能燃烧?实验III中火柴在铁丝上方,用其火焰内焰对铁丝加热,内焰温度低,没有对铁丝充分预热,因此不能达到铁丝的着火点.
(3)分析Ⅱ中铁丝燃烧比Ⅰ中更剧烈的原因:实验II中铁丝绕成螺旋状,与氧气接触面积增大,反应更充分.
探究二:铁粉腐蚀的条件
如图2所示,将所有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,观察到量筒内水沿着细导管慢慢进入广口瓶(容积为146mL).当温度恢复至室温,量筒内水面高度不变时读数(此时广口瓶内氧气含量几乎为零),记录量筒的起始和最终读数以及所需时间如下表:
| 序号 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
| ① | 1.0g铁粉、0.2g炭粉和10滴水 | 100 | 72 | 约120 |
| ② | 1.0g铁粉、0.2g炭粉、10滴水和少量NaCl | 100 | 72 | 约70 |
| ③ | / | / | / |
(2)实验开始后,广口瓶温度上升,说明铁锈蚀是放热(选填“放热”或“吸热”)过程.
(3)实验①和③是探究炭粉对铁锈蚀速率的影响,实验③表格空白处样品的组成是1g铁粉和10滴水.
(4)该装置还可用于测量空气中氧气的含量,根据上述数据计算得出空气中氧气的体积分数约是19.2%(精确到百分号前小数点后一位),试分析该实验结果出现误差的原因:滤纸包占有一定体积.
19. 在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行探究.
在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行探究.
[查阅资料]
(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成的.
(2)氯化钙、氯化钡溶液均呈中性.
[提出问题]
(l)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
[实验探究]
(1)按右图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论.此结论合理(选填“合理”或“不合理”).
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀.取沉淀于试管中加稀盐酸,有气泡产生.写出产生气体的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O.
分析实验并结合资料得出氢氧化钠已变质.
(3)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯中上层清液于两支试管中,按下图探究.
②乙组认为甲组实验不能证明清液中一定有氢氧化钠,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色.他们另取烧杯中上层清液,加足量氯化钡溶液,充分反应后滴加酚酞溶液,酚酞溶液变红.
[实验结论]经讨论一致认为固体酒精中的氢氧化纳部分变质.
[反思交流]乙组实验中加足量氯化钡溶液的目的是除去碳酸钠,防止影响对NaOH的检验.
[拓展应用]要除去部分变质的氢氧化纳溶液中的杂质,可选择适量的AC(填序号).
A.Ba(OH)2溶液 B.BaCl2溶液 C.Ca(OH)2溶液.
 在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行探究.
在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行探究.[查阅资料]
(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成的.
(2)氯化钙、氯化钡溶液均呈中性.
[提出问题]
(l)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
[实验探究]
(1)按右图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论.此结论合理(选填“合理”或“不合理”).
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀.取沉淀于试管中加稀盐酸,有气泡产生.写出产生气体的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O.
分析实验并结合资料得出氢氧化钠已变质.
(3)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯中上层清液于两支试管中,按下图探究.
| 方案 |  | 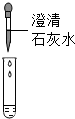 |
| 现象 | 溶液变红 | 产生 |
| 结论 | 清液有氢氧化钠 | 清液有碳酸钠 |
[实验结论]经讨论一致认为固体酒精中的氢氧化纳部分变质.
[反思交流]乙组实验中加足量氯化钡溶液的目的是除去碳酸钠,防止影响对NaOH的检验.
[拓展应用]要除去部分变质的氢氧化纳溶液中的杂质,可选择适量的AC(填序号).
A.Ba(OH)2溶液 B.BaCl2溶液 C.Ca(OH)2溶液.
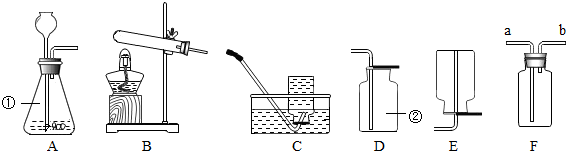
 实验室按下图所示装置制取CO2,并检验CO2的性质.试回答以下问题:
实验室按下图所示装置制取CO2,并检验CO2的性质.试回答以下问题: