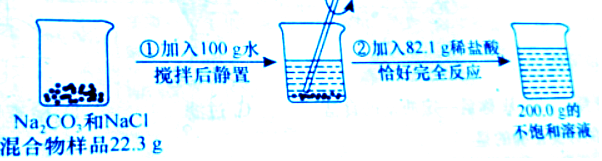
题目内容
15.人的胃液里含有适量盐酸.服用含MgCO3的抗酸药可治疗胃酸过多症,有关反应的化学方程式为MgCO3+2HCl=MgCl2+CO2↑+H2O;该抗酸药说明书上标明的食用方法为“嚼食”,将药片嚼碎后服用的优点是接触面积增大,反应速率加快,疗效好.医院在对病人做胃病透视检查时,往往要服用“钡餐”.“钡餐”的主要成分是硫酸钡.而可溶性钡盐有毒,若误服碳酸钡就会引起中毒,一旦中毒,需立即服用泻盐(硫酸镁)解毒.请写出解毒反应的化学方程式BaCl2+MgSO4═BaSO4↓+MgCl2.分析 MgCO3能与胃液中的盐酸反应生成氯化镁、水和二氧化碳,嚼碎后与反应物胃酸的接触面积增大,BaCO3能与胃液中的盐酸反应生成易溶于水的氯化钡、水和二氧化碳,生成的氯化钡易溶于水,会使人中毒;硫酸镁可以与BaCl2反应生成难溶于胃酸的BaSO4和无毒的氯化镁;据此进行分析解答.
解答 解:MgCO3能与胃液中的盐酸反应生成氯化镁、水和二氧化碳,反应的化学方程式为MgCO3+2HCl=MgCl2+CO2↑+H2O.
因嚼碎后与反应物胃酸的接触面积增大,反应速率加快,则嚼碎后服用疗效好.
BaCO3能与胃液中的盐酸反应生成易溶于水的氯化钡、水和二氧化碳,生成的氯化钡易溶于水,会使人中毒,中毒后可立即服用泻盐(硫酸镁)来解,是因为硫酸镁可以与BaCl2反应生成难溶于胃酸的BaSO4和无毒的氯化镁,反应的化学方程式为:BaCl2+MgSO4═BaSO4↓+MgCl2.
故答案为:MgCO3+2HCl=MgCl2+CO2↑+H2O;接触面积增大,反应速率加快,疗效好;BaCl2+MgSO4═BaSO4↓+MgCl2.
点评 本题难度不大,熟练掌握盐的化学性质、化学方程式的书写等并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
15.下列有关物质的提纯、除杂和鉴别所用的试剂或方法错误的是( )
| 选项 | 实验目的 | 所加物质或方法 |
| A | 除去CaO中的CaCO3 | 高温煅烧至固体质量不再改变 |
| B | 提纯硫酸钠中的硝酸钠 | 溶解、加适量的氯化钡溶液,过滤,蒸发 |
| C | 除去CO2中少量的HCl | 将混合气体通入饱和碳酸氢钠溶液,再通入浓硫酸 |
| D | 鉴别NH4NO3固体和NaOH固体 | 加水溶解 |
| A. | A | B. | B | C. | C | D. | D |
3.如图是某化学反应的微观示意图,其中“ ”和“
”和“ ”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质,下列关于该反应前、后的说法不正确的是( )
”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质,下列关于该反应前、后的说法不正确的是( )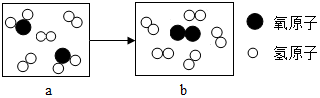
 ”和“
”和“ ”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质,下列关于该反应前、后的说法不正确的是( )
”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质,下列关于该反应前、后的说法不正确的是( )
| A. | 反应前后原子总数不变 | B. | a、b均为混合物 | ||
| C. | 该反应为分解反应 | D. | a中两种物质均为化合物 |
20.如表中各组物质的鉴别方法不正确的是
| 选项 | 需要鉴别的物质 | 鉴别方法 |
| A | 氮气、氧气、二氧化碳 | 用燃着的木条区分 |
| B | 氯化钠、硝酸铵、碳酸钙 | 加入足量的水 |
| C | 碳酸钾溶液、硝酸钡溶液、硫酸钾溶液 | 加入足量的稀硫酸 |
| D | 硫酸铜溶液、氢氧化钠溶液、氯化钾溶液 | 利用组内物质间的相互反应区分 |
| A. | A | B. | B | C. | C | D. | D |
 2016年11月3日,我国大推力运载火箭长征五号发射成功,我国具备了建造空间站的能力.
2016年11月3日,我国大推力运载火箭长征五号发射成功,我国具备了建造空间站的能力.