题目内容
7.请根据如图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),完成下列问题: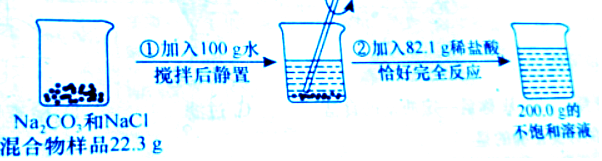
(1)该反应产生的CO2气体质量为4.4g
(2)计算原混合物中碳酸钠的质量分数(写出计算过程).
分析 碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;反应前后的质量差即为反应生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钠的质量,进一步可以计算原混合物中碳酸钠的质量分数.
解答 解:(1)生成二氧化碳的质量为:22.3g+100g+82.1g-200.0g=4.4g,
故填:4.4.
(2)设碳酸钠的质量为x,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 44
x 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$,
x=10.6g,
原混合物中碳酸钠的质量分数为:$\frac{10.6g}{22.3g}$×100%=47.5%,
答:原混合物中碳酸钠的质量分数为47.5%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
7.如表列出了一些常见物质在常温下的 pH 范围,其中呈碱性的是( )
| 物质名称 | 鸡蛋清 | 牛奶 | 西红柿 | 柠檬汁 |
| pH 范围 | 7.6~8.0 | 6.3~6.6 | 4.0~4.4 | 2.0~3.0 |
| A. | 鸡蛋清 | B. | 牛奶 | C. | 西红柿 | D. | 柠檬汁 |
12.将适量的碳酸钙粉末加入到盛有83.2克稀盐酸的烧杯中,立即将烧杯放在天平上称量.在以后的8min内,每一分钟读一次数(最后二者恰好完全反应).结果如下
请分析并解答下列问题(前3小题直接把答案写在横线处,第4小题写出解题过程):
(1)烧杯中物质质量减少的原因是反应生成的二氧化碳逸出
(2)在该反应中,会发现随着反应的进行,反应速度越来越小,这说明反应速度与反应物的浓度有关
(3)有表格可看出,反应完全结束的时间是在第6分钟
(4)计算反应后溶液的溶质质量分数.
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 质量/g | 93.2 | 91.4 | 90.2 | 89.5 | 89.1 | 88.9 | 88.8 | 88.8 | 88.8 |
(1)烧杯中物质质量减少的原因是反应生成的二氧化碳逸出
(2)在该反应中,会发现随着反应的进行,反应速度越来越小,这说明反应速度与反应物的浓度有关
(3)有表格可看出,反应完全结束的时间是在第6分钟
(4)计算反应后溶液的溶质质量分数.
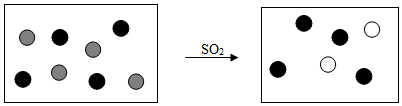
 ”表示Fe2+.(填写微粒的符号)
”表示Fe2+.(填写微粒的符号)