题目内容
5.某工厂排放的废水中含有硫酸,为了减少废水对环境的污染,需要用熟石灰来处理,若该工厂每天排放的废水中含196kg硫酸,需要用含量为74%的石灰浆将硫酸完全中和(假设废水中的其他成分不与熟石灰反应),请计算:(1)硫酸中硫元素的质量分数为32.7%;(结果精确到0.1%)
(2)至少消耗石灰浆的质量.
分析 根据物质的化学式可以计算组成元素的质量分数;
稀硫酸和氢氧化钙反应生成硫酸钙和水,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)硫酸的化学式是H2SO4,其中硫元素的质量分数为:$\frac{32}{98}$×100%=32.7%,
故填:32.7%.
(2)设至少消耗氢氧化钙的质量为x,
Ca(OH)2+H2SO4═CaSO4+2H2O,
74 98
x 196kg
$\frac{74}{x}$=$\frac{98}{196kg}$,
x=148kg,
至少消耗石灰浆的质量为:148kg÷74%=200kg,
答:至少消耗石灰浆的质量为200kg.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
20.2017年“世界水日”和“中国水周”活动的宣传主题为“落实绿色发展理念,全面推行河长制”,下列做法不符合这一主题的是( )
| A. | 加强水资源保护,落实最严格水资源管理制度 | |
| B. | 依法划定河湖管理范围,严格水域岸线等水生态空间管控 | |
| C. | 为了加快地方经济的发展,可以适当向河流中排放一些污染物 | |
| D. | 加强依法治水管水,推进水利依法行政 |
10.课本上有8个“基础实验”,以提升同学们的实验能力,以下叙述正确的是( )
| A. | “粗盐的初步提纯”实验中,持续加热食盐溶液直至水分蒸干 | |
| B. | “溶液的酸碱性”实验中,将pH试纸伸入溶液中测定酸碱度 | |
| C. | “氧气的制取与性质”实验中,做铁丝燃烧实验的集气瓶内要预留少量的水 | |
| D. | “酸与碱的化学性质”实验中,将实验废液直接倒入下水道 |
14.生活中的下列变化,属于物理变化的是( )
| A. | 植物的光合作用 | B. | 燃放烟花 | C. | 蜡烛燃烧 | D. | 灯泡发光 |
15.下列物质由原子直接构成的是( )
| A. | Fe | B. | H2O | C. | NaOH | D. | H2 |
 ”表示Fe2+.(填写微粒的符号)
”表示Fe2+.(填写微粒的符号)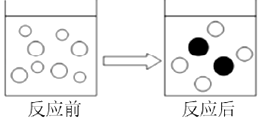
 固体氢氧化钠放置在空气中容易变质转化为碳酸钠.现称取一久置于空气中的烧碱样品12.6g完全溶于蒸馏水中配成100g溶液,向其中滴加质量分数为8.55%的氢氧化钡溶液,产生沉淀与所加氢氧化钡溶液的质量关系如图所示.请通过计算回答:
固体氢氧化钠放置在空气中容易变质转化为碳酸钠.现称取一久置于空气中的烧碱样品12.6g完全溶于蒸馏水中配成100g溶液,向其中滴加质量分数为8.55%的氢氧化钡溶液,产生沉淀与所加氢氧化钡溶液的质量关系如图所示.请通过计算回答: