题目内容
13.自来水厂净水过程的主要操作流程如图.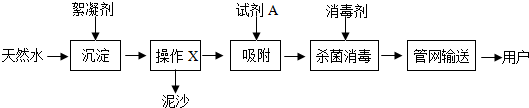
资料:常用的絮凝剂有明矾[KAl(SO4)•12H2O],消毒剂有液氯(Cl2)
回答下列问题:
(1)操作X的名称是明矾,试剂A的名称是活性炭.
(2)明矾作絮凝剂是因为与水反应生成氢氧化铝胶状物.氢氧化铝的化学式为Al(OH)3.液氯与水中杂质反应生成一些对人体有害的物质,例如三氯甲烷(CHCl3).三氯甲烷属于有机物(填“有机物”或“无机物”)
(3)高铁酸钾(K2FeO4)能作消毒剂与絮凝剂.它杀菌时会生成氢氧化铁胶状物.高铁酸钾中铁元素的化合价是+6价.
(4)自来水厂的净水过程不能(填“能”或“不能”)将硬水软化成软水.生活总将硬水软化的方法是煮沸,经过此法后,水中的部分Ca2+、Mg2+转化为沉淀,即通常所说的水垢,水垢的主要成分为碳酸钙和氢氧化镁.
(5)自来水中通常都含有Cl-,可以在水样中滴加少量稀硝酸和硝酸银溶液检验,若出现白色沉淀现象,说明水中含有Cl-.
(6)实验室用自来水制取蒸馏水的蒸馏烧瓶里,通常要加入几粒沸石或碎瓷片,作用是防止暴沸.
(7)自来水可被电解,电解水试验中,正、负极产生气的体积比V正极:V负极=1:2.
分析 (1)常见的净化水的方法按照净化程度由低到高的顺序是沉降、过滤、吸附、蒸馏等流程;根据吸附过程解答;
(2)根据物质化学式的写法解答;
(3)根据化合物中正负化合价的代数和为零解答;
(4)根据硬水中含有较多的钙、镁离子,加热煮沸可以将硬水软化成软水;
(5)根据氯离子的检验方法分析回答;
(6)根据蒸馏的原理及注意的事项分析;
(7)根据电解水的实验现象解结论分析解答.
解答 解:(1)在自来水厂为了将小颗粒泥尘沉降下来,常用絮凝剂,经常使用的絮凝剂是明矾,为了除去不溶于水的固体杂质,必须用过滤的方法;在过滤后的水中仍然含有可溶性的有色、有异味的物质,通常用吸附剂来吸附,吸附能力较强的是活性炭;
(2)氢氧化铝的化学式为:Al(OH)3;一般含有碳元素的化合物是有机物,三氯甲烷(CHCl3)属于有机物;
(3)化合物中正负化合价的代数和为零,设铁元素的化合价是x
(+1)×2+x+(-2)×4=0
x=+6
(4)自来水厂的净水过程不能将硬水软化成软水,生活中将硬水软化的方法煮沸.经过此法后,水中的部分Ca2+、Mg2+转化为沉淀,即通常所说的水垢,水垢的主要成分为碳酸钙和氢氧化镁;
(5)自来水中通常都含有Cl-,可以在水样中滴加少量稀硝酸和硝酸银检验,若出现白色沉淀现象,说明水中含有Cl-;
(6)把自来水进一步净化为蒸馏水的实验方法是蒸馏.实验室制取蒸馏水的蒸馏烧瓶里,通常要加入几粒沸石或碎瓷片,作用是防止暴沸.
(7)自来水可被电解,电解水试验中,正氧负氢,氢二氧一,正、负极产生气的体积比V正极:V负极=1:2
答案:
(1)过滤;活性炭;
(2)Al(OH)3;有机物;
(3)+6价;
(4)不能;煮沸;碳酸钙和氢氧化镁;
(5)硝酸银溶液; 白色沉淀;
(6)防止暴沸;
(7)1:2
点评 .本题难度不大,掌握水的净化方法、过滤操作、硬水和软水的检验以及电解水的实验操作即可正确解答本题.

 某同学利用如图装置进行两个实验.
某同学利用如图装置进行两个实验. | Ⅰ中药品 | Ⅱ中药品 | Ⅲ中药品 | |
| 实验1 | 鸡蛋壳、稀盐酸 | 澄清石灰水 | 紫色石蕊溶液 |
| 实验2 | MnO2、H2O2溶液 | 白磷 热水(80℃) | 白磷 冷水(10℃) |
下列说法不正确的是( )
| A. | 实验1,可观察到Ⅱ中澄清石灰水变浑浊,Ⅲ中的紫色石蕊溶液变红 | |
| B. | 实验1,通过对实验过程的观察分析,能说明产物中有CO2气体 | |
| C. | 实验2,装置Ⅱ、Ⅲ中均有气泡产生,试管Ⅱ中的白磷发生燃烧 | |
| D. | 实验2,通过对实验过程的观察分析,只能证明可燃物燃烧的一个条件 |
| A. | 硫酸铜、氯化钠、纯碱-盐 | B. | 硫酸铵、草木灰、尿素-氮肥 | ||
| C. | 空气、天然气、碘酒-混合物 | D. | 铁元素、铜元素、汞元素-金属元素 |
| A. | 0.8 | B. | 1 | C. | 1.5 | D. | 无法确定 |
| A. | 黄铜、塑料、玻璃属于合成材料 | |
| B. | 纯喊、干冰、稀有气体属于化合物 | |
| C. | 硝酸钾、磷酸二氢铵、氯化铵属于复合肥 | |
| D. | 铜丝、石墨、食盐水属于导体 |

