题目内容
5.镁铝合金xg和足量盐酸反应生成0.1gH2,则x可能为( )| A. | 0.8 | B. | 1 | C. | 1.5 | D. | 无法确定 |
分析 根据氢气的质量分别求出所需镁与铝的质量,则x在这两个值之间.
解答 解:假设氢气全由镁与盐酸反应制取
设需要镁的质量为y,
Mg+2HCl═MgCl2+H2↑
24 2
y 0.1g
$\frac{24}{x}$=$\frac{2}{0.1g}$
y=1.2g
假设氢气全由铝与盐酸反应制取
设需要铝的质量为z
2Al+6HCl═2AlCl3+3H2↑
54 6
z 0.1g
$\frac{54}{z}$=$\frac{6}{0.1g}$
z=0.9g
因固体是镁与铝的混合物,所以X的取值范围为0.9g<x<1.2g
故选:B.
点评 本题主要考查学生利用化学方程式进行计算和分析的能力.解题的关键是分析两种金属都与足量的酸反应,生成0.1克氢气所需的质量关系.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
8.下列实验操作或现象正确的是( )
| A. | 排水法收集氧气时,当导管口开始有气泡冒出时立即收集 | |
| B. | 氢气、甲烷等可燃性气体点燃前进行验纯 | |
| C. | 用红磷燃烧来测定空气中氧气含量时,出现大量白雾,冷却后水倒吸约$\frac{1}{5}$体积 | |
| D. | 稀释浓硫酸时,沿烧杯壁将水缓缓注入盛有浓硫酸的烧杯中,并用玻璃棒不断搅拌 |
20.下列对一些事实的解释中,不合理的是( )
| 选项 | 事实 | 解释 |
| A | 0.0151m3的钢瓶可以装入20m3的气体,但是只能装入0.015m3的水 | 气体分子之间有间隔,液态分子间没有间隔 |
| B | 将墨汁滴入一杯淸水中,清水很快变黑 | 分子在不断运动 |
| C | 1滴水的质量的为0.05g,大约含有1.67×l021个水分子 | 分子的质量和体积都很小 |
| D | 过氧化氢受热分解,水受热不分解 | 二者分子构成不同,分子是保持物质化学性质的最小微粒 |
| A. | A | B. | B | C. | C | D. | D |
10.下列对实验现象的描述中,正确的是( )
| A. | 红磷在空气中燃烧,产生大量白雾 | |
| B. | 高锰酸钾溶于汽油,溶液呈紫红色 | |
| C. | 聚乙烯塑料加热时熔化,冷却后变成固体,加热后又熔化 | |
| D. | 电解水实验中,用燃着的木条检验正极端玻璃管中的气体,木条熄灭 |
17.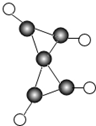 科学家最近在-100℃的低温下合成了一种化合物X,此分子的模型如图所示,其中每个“●”代表一个碳原子,每个“○”代表一个氢原子,下列说法中不正确的是( )
科学家最近在-100℃的低温下合成了一种化合物X,此分子的模型如图所示,其中每个“●”代表一个碳原子,每个“○”代表一个氢原子,下列说法中不正确的是( )
 科学家最近在-100℃的低温下合成了一种化合物X,此分子的模型如图所示,其中每个“●”代表一个碳原子,每个“○”代表一个氢原子,下列说法中不正确的是( )
科学家最近在-100℃的低温下合成了一种化合物X,此分子的模型如图所示,其中每个“●”代表一个碳原子,每个“○”代表一个氢原子,下列说法中不正确的是( )| A. | 该分子的化学式为C5H4 | |
| B. | 该分子中碳元素的质量分数为93.75% | |
| C. | 该分子中的碳原子与氢原子的原子个数比为5:4 | |
| D. | 等质量的该物质与甲烷相比,燃烧时消耗的氧气更多 |
14.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH═Na2SO4 +2H2O.
【提出问题】实验未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
【猜想假设】针对疑问,太家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四.
【实验探究】:
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH或氢氧化钠.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们用多种方法进行探究,并得出正确结论给予肯定.同时指出
实验探究(2)中存在两处明显错误,请大家反思.同学们经过反思发现了两处错误:
①实验操作中的错误是pH试纸浸入溶液中.
②实验方案中有一个是错误的,写出能说明实验方案错误原因的化学方程式BaCl2+Na2SO4═BaSO4↓+2NaCl.
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH═Na2SO4 +2H2O.
【提出问题】实验未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
【猜想假设】针对疑问,太家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是猜想四.
【实验探究】:
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH或氢氧化钠.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 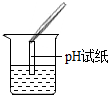 |  |  |
| 实验现象 | 试纸变色,对比比色卡, pH<7(选填“>、<、=”) | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师对同学们用多种方法进行探究,并得出正确结论给予肯定.同时指出
实验探究(2)中存在两处明显错误,请大家反思.同学们经过反思发现了两处错误:
①实验操作中的错误是pH试纸浸入溶液中.
②实验方案中有一个是错误的,写出能说明实验方案错误原因的化学方程式BaCl2+Na2SO4═BaSO4↓+2NaCl.