题目内容
4.往AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生.根据上述现象分析,你认为下面结论错误的是( )| A. | 滤渣一定有Fe粉 | B. | 滤渣一定有Cu粉 | ||
| C. | 滤液中一定有Fe2+ | D. | 滤液中一定有Ag+、Cu2+ |
分析 根据金属银、铜、铁的活动性由强到弱的顺序铁>铜>银,当把铁粉加入到AgNO3和Cu(NO3)2的混合溶液中,首先置换出银,银被置换完才继续置换铜;过滤后向滤渣中滴加稀盐酸,有气泡产生,说明加入的铁已全部发生了反应.
解答 解:由题意可知,向滤渣中加入稀盐酸,有气泡产生,说明加入的铁有剩余,则一定有银、铜被置换出来;由于铁粉过量,所以硝酸铜、硝酸银全部参加反应;因此,只能得到滤液中一定含有Fe(NO3)2,滤渣中一定含有Ag、Fe、Cu的结论.由以上分析可知:
A、滤渣中一定有Fe粉,故A正确;
B、滤渣中一定含有Cu,故B正确;
C、滤液中一定有Fe2+,故C正确;
D、滤液中一定没有Ag+、Cu2+,故D错误.
故选:D.
点评 金属放入盐的混合溶液中,首先把活动性最弱的金属置换出来,置换的先后顺序为由弱到强,最强的最后置换出来.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
15.实验室部分装置如图所示,请回答有关问题.

(1)写出a、b两种仪器的名称:a长颈漏斗,b锥形瓶.
(2)实验室用过氧化氢溶液和二氧化锰粉末制取氧气,最好选择图中的AF(填编号)组装一套制取装置,反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.装入药品前必须进行的一步操作是检查装置气密性.
(3)小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题.她进行了如下实验探究:
①请你帮小丽同学填写上表中未填完的空格.
②小英同学认为仅由上述实验还不能完全证明命题的成立,她补充设计了如下探究,最终完成了对“命题”的实验证明.
探究1:在实验三开始和结束时,分别称量二氧化锰的质量,其目的是证明MnO2在过氧化氢分解前后的质量不变;
探究2:利用实验三反应后试管内的剩余物继续实验.接下来的实验操作、现象和结论是倒掉反应后的液体,向剩余的固体中重新加入过氧化氢溶液,有大量气泡产生,证明MnO2仍能加快过氧化氢的分解速率,化学性质也没变.

(1)写出a、b两种仪器的名称:a长颈漏斗,b锥形瓶.
(2)实验室用过氧化氢溶液和二氧化锰粉末制取氧气,最好选择图中的AF(填编号)组装一套制取装置,反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.装入药品前必须进行的一步操作是检查装置气密性.
(3)小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题.她进行了如下实验探究:
| 实验一 | 实验二 | 实验三 | |
| 实验操作 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 取5mL水于试管中,加入二氧化锰,伸入带火星的木条 | 取5mL5%过氧化氢溶液放入试管中,加入二氧化锰,伸入带火星的木条 |
| 实验现象 | 有气泡产生,木条不复燃 | 没有明显现象 | 有大量气泡产生,带火星的木条迅速复燃 |
| 实验结论 | 过氧化氢分解产生氧气速度较慢 | 二氧化锰加入水中不产生氧气 | 二氧化锰能加快过氧化氢的分解 |
| 二氧化锰是过氧化氢分解的催化剂 | |||
②小英同学认为仅由上述实验还不能完全证明命题的成立,她补充设计了如下探究,最终完成了对“命题”的实验证明.
探究1:在实验三开始和结束时,分别称量二氧化锰的质量,其目的是证明MnO2在过氧化氢分解前后的质量不变;
探究2:利用实验三反应后试管内的剩余物继续实验.接下来的实验操作、现象和结论是倒掉反应后的液体,向剩余的固体中重新加入过氧化氢溶液,有大量气泡产生,证明MnO2仍能加快过氧化氢的分解速率,化学性质也没变.
12.如图为甲生成乙和丙的反应示意图,其中丙是呼吸作用产物之一,则( )
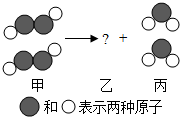

| A. | 该反应是化合反应 | B. | 甲是有机物 | ||
| C. | 甲的相对分子质量为34g | D. | 乙由一种元素组成 |
13.物质之间存在联系,找出联系,发现规律是我们学好化学的一种基本方法.
(1)请你仿照下表中的示例,找出CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体之间存在的另外两个规律并排序.
(2)某气体由CH4、C2H2、C2H4中的一种或几种组成,取该气体样品在氧气中完全燃烧,测得生成的二氧化碳和水的质量比为22:9,下列对该气体组成判断正确的是C.
A.该气体中一定含有C2H4
B.该气体中一定没有CH4
C.该气体中可能含有C2H2
D.该气体不可能同时含有CH4、C2H2、C2H4.
(1)请你仿照下表中的示例,找出CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体之间存在的另外两个规律并排序.
| 规律 | 排序 |
| 示例:标准状况下,密度由大到小 | CO2、C2H4、C2H2、CH4 |
A.该气体中一定含有C2H4
B.该气体中一定没有CH4
C.该气体中可能含有C2H2
D.该气体不可能同时含有CH4、C2H2、C2H4.
14.不能达到相应实验目的装置是( )
| A. | 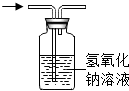 除去一氧化碳中的二氧化碳 | B. | 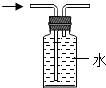 排水法收集氢气 | ||
| C. | 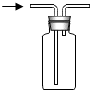 向上排空气法收集氧气 | D. |  检验氢气中是否混有氯化氢 |
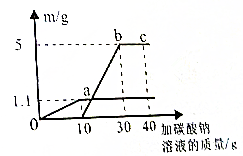 小红取实验时制CO2反应后的废液50g(含有CaCl2和HCl),逐滴加入碳酸钠溶液.他根据实验测得的数据绘出如图,其中纵坐标m是实验得到的沉淀或气体的质量,横坐标表示的是碳酸钠溶液质量
小红取实验时制CO2反应后的废液50g(含有CaCl2和HCl),逐滴加入碳酸钠溶液.他根据实验测得的数据绘出如图,其中纵坐标m是实验得到的沉淀或气体的质量,横坐标表示的是碳酸钠溶液质量