题目内容
16.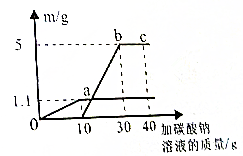 小红取实验时制CO2反应后的废液50g(含有CaCl2和HCl),逐滴加入碳酸钠溶液.他根据实验测得的数据绘出如图,其中纵坐标m是实验得到的沉淀或气体的质量,横坐标表示的是碳酸钠溶液质量
小红取实验时制CO2反应后的废液50g(含有CaCl2和HCl),逐滴加入碳酸钠溶液.他根据实验测得的数据绘出如图,其中纵坐标m是实验得到的沉淀或气体的质量,横坐标表示的是碳酸钠溶液质量(1)废液中oa段表示的是生成的CO2(填化学式)质量为1.1g
(2)废液中所含HCl的质量分数
(3)耗去碳酸钠溶液中溶质的质量.
分析 根据已有的知识进行分析,大理石和盐酸反应后生成氯化钙,可能存在剩余的盐酸,碳酸钠能与盐酸反应生成二氧化碳气体,碳酸钠能与氯化钙反应生成碳酸钙沉淀,碳酸钙能与盐酸反应生成氯化钙,故在盐酸存在的情况下,碳酸钠首先与盐酸反应,据此解答即可.
解答 解:根据图象可以看出,加入碳酸钠溶液时,溶液中出现两个反应,大理石和盐酸反应后生成氯化钙,可能存在剩余的盐酸,碳酸钠能与盐酸反应生成二氧化碳气体,碳酸钠能与氯化钙反应生成碳酸钙沉淀,碳酸钙能与盐酸反应生成氯化钙,故在盐酸存在的情况下,碳酸钠首先与盐酸反应,所以在废液中含有剩余的盐酸和生成的氯化钙;
(1)在盐酸存在的情况下,碳酸钠首先与盐酸反应,故oa段表示生成的二氧化碳气体的质量,
(2)与碳酸钠反应的盐酸能够生成1.1g二氧化碳,
设含氯化氢的质量为x,消耗碳酸钠的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 44
y x 1.1g
$\frac{73}{x}$=$\frac{44}{1.1g}$
x=1.825g
$\frac{106}{y}$=$\frac{44}{1.1g}$
y=2.65g
盐酸的质量分数为:$\frac{1.825g}{25g}$×100%=7.3%,
(3)由(2)可知耗去碳酸钠溶液质量为10g时含碳酸钠2.65g,所以耗去30g碳酸钠溶液中溶质的质量为2.65g×3=7.95g
故答案为:(1)CO2(2)7.3%(3)7.95g
点评 本题考查了混合溶液中的物质间的复分解反应与图象的结合关系,完成此题,可以依据已有的知识结合物质的性质进行.要求同学们熟记有关物质的性质,以便灵活应用.

练习册系列答案
相关题目
4.往AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生.根据上述现象分析,你认为下面结论错误的是( )
| A. | 滤渣一定有Fe粉 | B. | 滤渣一定有Cu粉 | ||
| C. | 滤液中一定有Fe2+ | D. | 滤液中一定有Ag+、Cu2+ |
11.汽油机是以汽油为燃料的一种内燃机,燃烧产物中含有大量对环境污染的物质.一种新型燃料的混合使用,使得上述问题有望得到缓解.已知一定量的新型燃料完全燃烧产生8.8克CO2和5.4克H2O,请判断该新型燃料可能是( )
| A. | CH3OH | B. | C2H5OH | C. | C6H12O6 |
5.如图是四种微粒结构示意图,下列有关各微粒的说法中,错误的是( )
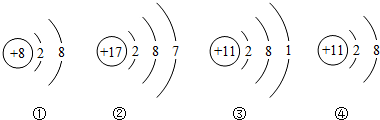
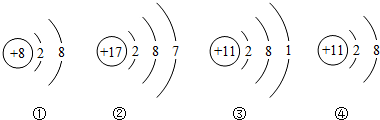
| A. | ①的化学性质比较稳定 | B. | ③④属于同种元素 | ||
| C. | ④是一种阴离子 | D. | ②容易得到电子 |

 如图是初中化学常见物质间的转化关系(反应条件和部分产物已略去),其中A为钠盐,X,Y均为黑色粉末,D为红色金属单质,F在常温下为液态,回答下列问题.
如图是初中化学常见物质间的转化关系(反应条件和部分产物已略去),其中A为钠盐,X,Y均为黑色粉末,D为红色金属单质,F在常温下为液态,回答下列问题.