题目内容
13.物质之间存在联系,找出联系,发现规律是我们学好化学的一种基本方法.(1)请你仿照下表中的示例,找出CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体之间存在的另外两个规律并排序.
| 规律 | 排序 |
| 示例:标准状况下,密度由大到小 | CO2、C2H4、C2H2、CH4 |
A.该气体中一定含有C2H4
B.该气体中一定没有CH4
C.该气体中可能含有C2H2
D.该气体不可能同时含有CH4、C2H2、C2H4.
分析 根据化学式表示意义,可从相对分子质量的大小,一个分子中所含原子个数的多少等来寻找规律;根据二氧化碳和水的质量比为22:9,可计算出碳、氢两种元素的质量比,据此解答.
解答 解:(1)CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体相对分子质量分别是:44,16,26,28;所以相对分子质量由小到大的顺序是CH4、C2H2、C2H4、CO2.
CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体一个分子中所含原子个数分别是3,5,4,6;所以一个分子分子中所含原子个数由少到多的顺序是CO2、C2H2、CH4、C2H4.
故答案为:
| 规律 | 排列顺序 |
| 标准状况下,相对分子质量由小到大 | CH4、C2H2、C2H4、CO2 |
| 每个分子中含的原子总数由小到多 | CO2、C2H2、CH4、C2H4 |
A.若是含一个CH4和一个C2H2,则能达到碳氢原子个数比是1:2,该气体中不一定含有C2H4,错误;
B.若是含一个CH4和一个C2H2,则能达到碳氢原子个数比是1:2,错误;
C.该气体中可能含有C2H2,正确;
D.该气体可能同时含有CH4、C2H2、C2H4,错误;
故填C.
点评 主要考查了相对分子质量的计算和分子的构成.根据化学式进行有关的推断时,要结合质量守恒定律以及化学式的有关计算进行.

练习册系列答案
相关题目
4.往AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生.根据上述现象分析,你认为下面结论错误的是( )
| A. | 滤渣一定有Fe粉 | B. | 滤渣一定有Cu粉 | ||
| C. | 滤液中一定有Fe2+ | D. | 滤液中一定有Ag+、Cu2+ |
5.如图是四种微粒结构示意图,下列有关各微粒的说法中,错误的是( )
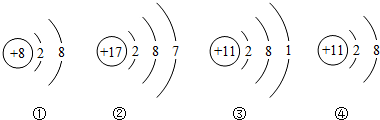
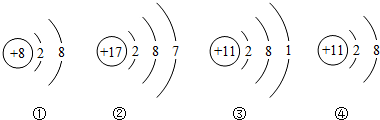
| A. | ①的化学性质比较稳定 | B. | ③④属于同种元素 | ||
| C. | ④是一种阴离子 | D. | ②容易得到电子 |
2.下列各组离子可在同一溶液中大量共存的是( )
| A. | H+ SO${\;}_{4}^{2-}$、K+、CO${\;}_{3}^{2-}$ | B. | Mg2+、Cl-、OH-、Na+ | ||
| C. | Fe3+、SO${\;}_{4}^{2-}$、H+、Cl- | D. | Na+、Ba2+、NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$ |
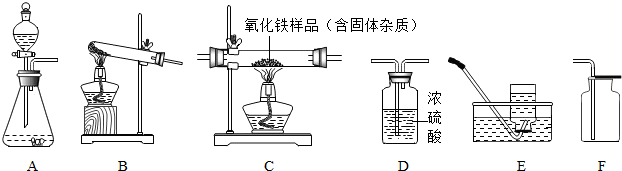
 如图是初中化学常见物质间的转化关系(反应条件和部分产物已略去),其中A为钠盐,X,Y均为黑色粉末,D为红色金属单质,F在常温下为液态,回答下列问题.
如图是初中化学常见物质间的转化关系(反应条件和部分产物已略去),其中A为钠盐,X,Y均为黑色粉末,D为红色金属单质,F在常温下为液态,回答下列问题.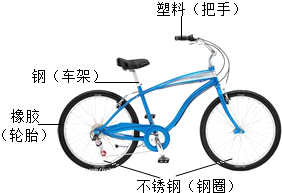 自行车作为常用的代步工具,既轻便灵活,又符合环保要求.如图是一款自行车的示意图.
自行车作为常用的代步工具,既轻便灵活,又符合环保要求.如图是一款自行车的示意图.