题目内容
2.(1)在二氧化碳、水、铁和氯化钠4种物质中,由分子构成的是二氧化碳、水.(2)碳酸氢钙的化学式为Ca(ClO2)2,其中氯元素的化合价是+1.
(3)在一密闭容器中,某反应前后的分子种类示意图如图1所示:
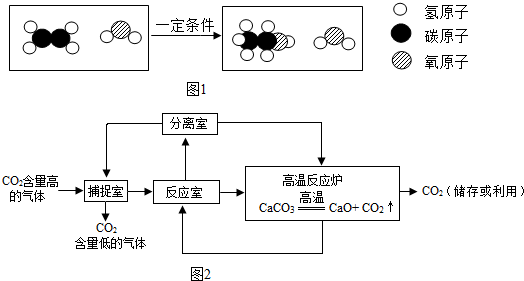
①生成物中各元素的质量比为碳氢氧元素的质量比为12:3:8.
②该反应的化学方程式是C2H4+H2O $\frac{\underline{\;一定条件\;}}{\;}$C2H6O.
(4)为防止二氧化碳过多排放到空气中,在实际生产中经常利用NaOH溶液来“捕捉”CO2,流程图如图2.则反应室内发生反应的化学方程式为C02+2NaOH=Na2C03+H20.
分析 (1)根据金属、大多数固态非金属单质等由原子构成,有些物质是由分子构成的,如水、氢气等,有些物质是由离子构成的,如氯化钠,进行分析解答;
(2)根据在化合物中正负化合价代数和为零,结合次氯酸钙的化学式进行解答本题;
(3)根据反应的微观示意图进行分析解答即可.
(4)根据反应物、生成物以及质量守恒定律写出方程式;
解答 解:(1)二氧化碳是由二氧化碳分子构成的;水是由水分子构成的;铁是由铁原子构成的;氯化钠是由钠离子和氯离子构成的.答案:二氧化碳、水;
(2)钙元素显+2价,氧元素显-2价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+2)+2x+(-2)×2=0,则x=+1价.答案:+1;
(3)①含有碳元素的生成物的化学式是C2H6O,故碳氢氧元素的质量比为:12×2:1×6:16=12:3:8,故填:碳氢氧元素的质量比为12:3:8;
②该化学反应是C2H4+H2O $\frac{\underline{\;一定条件\;}}{\;}$C2H6O,故填:C2H4+H2O $\frac{\underline{\;一定条件\;}}{\;}$C2H6O.
(4)二氧化碳和氢氧化钠反应生成碳酸钠和水,所以捕捉室内反应的化学方程式为:C02+2NaOH=Na2C03+H20;
故答案为:C02+2NaOH=Na2C03+H20;
点评 本题考查了物质构成和质量守恒定律的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案
相关题目
10.如表是氯化钠和硝酸钾在不同温度时的溶解度:
(1)从表中,可获取的一条信息是NaCl的溶解度受温度的变化影响不大等.
(2)60℃时,把113.3g KNO3和20g NaCl全部放入100g水中,充分溶解后形成KNO3和NaCl的不饱和溶液(填“饱和溶液”或“不饱和溶液”),降温至0℃时,溶液中NaCl的质量是20g,析出KNO3的质量是96.7g.由此得出从KNO3和NaCl的混合溶液中KNO3提纯的方法是降温结晶.
| 温度 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ | |
| 溶解度 | NaCl | 35.7g | 36.0g | 36.6g | 37.3g | 38.4g |
| KNO3 | 13.3g | 31.6g | 63.9g | 110g | 169g | |
(2)60℃时,把113.3g KNO3和20g NaCl全部放入100g水中,充分溶解后形成KNO3和NaCl的不饱和溶液(填“饱和溶液”或“不饱和溶液”),降温至0℃时,溶液中NaCl的质量是20g,析出KNO3的质量是96.7g.由此得出从KNO3和NaCl的混合溶液中KNO3提纯的方法是降温结晶.
7.下列各组物质按酸、碱、盐、单质、氧化物顺序排列的是( )
| A. | H2SO4 Na2O MgCl2 C CO | B. | Mg(OH)2 CuSO4 CaO C CO2 | ||
| C. | MgSO4 KOH NaCl O2 SO3 | D. | HCl NaOH NH4Cl O2 P2O5 |
14.下列各组离子在溶液中不能大量共存的是( )
| A. | H+ Ba2+ NO3- SO42- | B. | H+ NO3- Cl- Ca2+ | ||
| C. | K+ Mg2+ NO3- Cl- | D. | K+ Na+ Mg2+ SO42- |
11.酸、碱、盐在工农业生产和日常生活中的广泛应用,促进了人类文明的进步和社会的可持续发展.下列有关酸、碱、盐的生产或应用的说法不合理的是( )
| A. | 高温煅烧石灰石可制得生石灰 | |
| B. | 将草木灰(含K2CO3)与氯化铵混合施用 | |
| C. | 纯碱既可从内陆盐湖提取,又可用“侯氏联合制碱法”生产 | |
| D. | 用石灰乳与硫酸铜溶液混合配制防治植物病害的波尔多液 |
12.实验室里几种物质在互相谈论.你认为它们的叙述中属于化学变化的是( )
| A. | 试管:同学们不爱惜我,我被摔碎了 | |
| B. | 铁钉:好难受啊,我在潮湿空气中生锈了 | |
| C. | 灯泡:我通电后发光了,给学生带来光明 | |
| D. | 蜡烛:我受热就会熔化,遇冷我又会凝固 |