题目内容
3.证明集气瓶中盛有的是氧气,最简便的方法( )| A. | 能使蜡烛燃烧的是氧气 | |
| B. | 放入发红的木炭过一会儿加入澄清石灰水,可使澄清石灰水变浑浊 | |
| C. | 测定密度,如密度大于1的就是氧气 | |
| D. | 放入带火星的木条,可使木条复燃的是氧气 |
分析 A、根据空气也能使蜡烛燃烧考虑.
B、根据发红的木炭在氧气中不能燃烧考虑.
C、二氧化碳的密度也比1大.
D、根据氧气的助燃性考虑.
解答 解:A、蜡烛也能在空气中燃烧,故本选项错误;
B、发红的木炭在氧气中不能燃烧,不能判断是否含有氧气,故本选项错误;
C、密度大于1的气体不一定是氧气,例如二氧化碳的密度比1大,故本选项错误;
D、由于氧气具有助燃性,能使带火星的木条复燃,所以放入带火星的木条,可使木条复燃的是氧气,故本选项正确.
故选:D.
点评 本考点考查了空气中各种气体的含量和氧气的特性,同学们要加强记忆有关的知识点,在理解的基础上加以应用,本考点基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
11.为了测定某石灰石中碳酸钙的质量分数.取石灰石样品,与足量质量分数为7.3%的稀盐酸在烧杯(烧杯质量为20g)中充分反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水).有关实验数据如下表:
(1)配制上述质量分数为7.3%的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是20g;
(2)发生反应的化学方程式为CaC03+2HCl=CaCl2+H20+C02↑;
(3)求解llg该石灰石样品中碳酸钙质量(x)的比例式为$\frac{100}{x}=\frac{44}{4.4g}$;
(4)向反应后所得溶液中加入5.4g水后,则最终溶液中溶质的质量分数是10%;
(5)该水泥厂用该石灰石制得生石灰56t,理论上需要该石灰石的质量是66t.
| 反应前 | 反应后 | ||
| 实验 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和混合物的质量 |
| 数据 | 120g | 11g | 126.6g |
(2)发生反应的化学方程式为CaC03+2HCl=CaCl2+H20+C02↑;
(3)求解llg该石灰石样品中碳酸钙质量(x)的比例式为$\frac{100}{x}=\frac{44}{4.4g}$;
(4)向反应后所得溶液中加入5.4g水后,则最终溶液中溶质的质量分数是10%;
(5)该水泥厂用该石灰石制得生石灰56t,理论上需要该石灰石的质量是66t.
8.下表为元素周期表中某一周期元素的原子结构示意图.请回答下列问题:
(1)表中磷元素属于非金属(填金属或非金属)元素.
(2)表中具有相对稳定结构的元素是Ar.(填元素符号)
(3)表中与氧原子具有相同化学性质的是硫(填元素名称).
(1)表中磷元素属于非金属(填金属或非金属)元素.
(2)表中具有相对稳定结构的元素是Ar.(填元素符号)
(3)表中与氧原子具有相同化学性质的是硫(填元素名称).
| 元素名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 | 氩 |
| 元素符号 | Na | Mg | Al | Si | P | S | Cl | Ar |
| 原子结构示意图 | 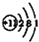 | 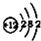 | 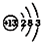 | 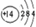 | 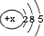 | 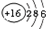 | 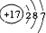 | 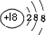 |
 某石灰石中含有杂质(杂质不溶于水,也不与盐酸反应),一兴趣小组想测定该样品中碳酸钙的质量分数,他们将一块样品敲打粉碎后,称出6g放入质量为20g的烧杯中,然后加入50g稀盐酸,用玻璃棒搅拌至不再产生气泡(盐酸有剩余),反应所需时间和烧杯及其所盛物质的总质量变化如图所示图:
某石灰石中含有杂质(杂质不溶于水,也不与盐酸反应),一兴趣小组想测定该样品中碳酸钙的质量分数,他们将一块样品敲打粉碎后,称出6g放入质量为20g的烧杯中,然后加入50g稀盐酸,用玻璃棒搅拌至不再产生气泡(盐酸有剩余),反应所需时间和烧杯及其所盛物质的总质量变化如图所示图: 向试管中加入适量硝酸铵,把试管固定在盛有饱和硝酸钾(室温下)的烧杯中,
向试管中加入适量硝酸铵,把试管固定在盛有饱和硝酸钾(室温下)的烧杯中, 研究性学习小组的同学为探究空气中氧气的体积分数,设计了如图所示装置.请根据图示实验回答下列问题.
研究性学习小组的同学为探究空气中氧气的体积分数,设计了如图所示装置.请根据图示实验回答下列问题.