题目内容
8.下表为元素周期表中某一周期元素的原子结构示意图.请回答下列问题:(1)表中磷元素属于非金属(填金属或非金属)元素.
(2)表中具有相对稳定结构的元素是Ar.(填元素符号)
(3)表中与氧原子具有相同化学性质的是硫(填元素名称).
| 元素名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 | 氩 |
| 元素符号 | Na | Mg | Al | Si | P | S | Cl | Ar |
| 原子结构示意图 | 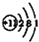 | 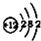 | 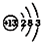 | 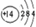 | 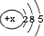 | 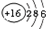 | 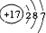 | 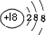 |
分析 (1)依据元素的命名特点分析解答;
(2)最外层具有8个电子的原子具有相对稳定结构.
(3)最外层电子数相同的化学性质相似,据此进行分析解答
解答 解:(1)根据磷元素的名称中含有“石”所以可知它是非金属元素;
(2)最外层具有8个电子的原子具有相对稳定结构,表中具有相对稳定结构的元素氩元素.
(3)氧原子的最外层电子数为6,与硫元素的最外层电子数相同故化学性质相似.
答案:(1)非金属;(2)Ar;(3)硫.
点评 本题难度不大,考查学生对原子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是正确解题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.把白糖和味精分别放在铁片上高温加热,结果都出现碳黑.仅根据此实验,可以得出的结论是( )
| A. | 两者尽管味道不同,实际上是相同的物质 | |
| B. | 两者都含碳元素 | |
| C. | 两者都含碳、氧元素 | |
| D. | 两者都含碳、氮、氧元素 |
19.小松同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的.他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动.
猜想与假设】小松同学猜想:Cr>Al>Cu;小雷同学猜想:Al>Cr>Cu
小聪同学猜想:Al>Cu>Cr
【查阅材料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液
【实验设计】同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量的稀硫酸中反应,观察现象.
【操作分析】三种金属加入稀硫酸前都先用砂布将表面擦光亮,其目的是(1)除去金属表面氧化物(或污物)
实验现象】
【实验结论】三种金属的金属活动性由强至弱的顺序,(2)小雷同学猜想正确.
【回答问题】小松提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小雷认为不可行,理由是(3)无法比较铬和铝的金属活动性强弱.
小聪认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是(4)A1、CrSO4溶液、Cu.
【归 纳】通过上述实验,可得出比较金属活动性强弱的方法有(5)金属与酸发生置换反应;金属与盐发生置换反应.
猜想与假设】小松同学猜想:Cr>Al>Cu;小雷同学猜想:Al>Cr>Cu
小聪同学猜想:Al>Cu>Cr
【查阅材料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液…铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液
【实验设计】同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量的稀硫酸中反应,观察现象.
【操作分析】三种金属加入稀硫酸前都先用砂布将表面擦光亮,其目的是(1)除去金属表面氧化物(或污物)
实验现象】
| 金属 | Cr | Al | Cu |
| 与硫酸反应现象 | 反应缓慢 | 反应剧烈 | 无明显现象 |
【回答问题】小松提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小雷认为不可行,理由是(3)无法比较铬和铝的金属活动性强弱.
小聪认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是(4)A1、CrSO4溶液、Cu.
【归 纳】通过上述实验,可得出比较金属活动性强弱的方法有(5)金属与酸发生置换反应;金属与盐发生置换反应.
3.证明集气瓶中盛有的是氧气,最简便的方法( )
| A. | 能使蜡烛燃烧的是氧气 | |
| B. | 放入发红的木炭过一会儿加入澄清石灰水,可使澄清石灰水变浑浊 | |
| C. | 测定密度,如密度大于1的就是氧气 | |
| D. | 放入带火星的木条,可使木条复燃的是氧气 |
 如图是童童同学在实验室里用一种纯净物制取氧气的装置图.请按要求回答下列问题.
如图是童童同学在实验室里用一种纯净物制取氧气的装置图.请按要求回答下列问题. 实验是进行科学探究的重要途径.在探究过程中,很多因素都会对实验结果产生影响.
实验是进行科学探究的重要途径.在探究过程中,很多因素都会对实验结果产生影响.