题目内容
11.张南同学取某种品牌的胃药30克放入烧杯中,再加入82克的稀盐酸,充分反应后所得混合物的质量为103.2克,此时溶液的PH=7.若此胃药中只含氢氧化铝、氧化镁、碳酸氢钠等常见的治疗胃病药剂中的一种,且胃药中的其他成分不与盐酸反应也不溶于水,求:(1)反应中生成的气体质量为8.8克.
(2)充分反应后混合物中固体的质量为13.2g克.
(3)反应后所得溶液溶质的质量分数为多少?(要求写出规范的计算过程)
分析 30克胃药与82克盐酸混合,充分反应后只得到103.2克混合物,少了8.8克,说明生成了8.8气体,由于在氢氧化铝、氧化镁、碳酸氢钠,只有碳酸氢钠与盐酸反应能生成气体;根据二氧化碳的质量计算碳酸氢钠的质量和氯化钠的质量,进而求混合物中固体的质量和反应后所得溶液溶质的质量分数.
解答 解:(1)反应中生成的气体质量为:30g+82g-103.2g=8.8g;
故填:8.8 g;
解:设碳酸氢钠的质量为x,同时生成NaCl质量为y
NaHCO3+HCl=NaCl+H2O+CO2↑
84 58.5 44
x y 8.8g
$\frac{84}{x}=\frac{58.5}{y}=\frac{44}{8.8g}$
x=16.8g,y=11.7g
(2)充分反应后混合物中固体的质量为:30g-16.8g=13.2g;
故填:13.2g;
(3)反应后所得溶液溶质的质量分数为:$\frac{11.7g}{103.2g-13.2g}×100%$=13%
答:反应后所得溶液溶质的质量分数为13%.
点评 主要考查了酸的化学性质,常见化学方程式的书写,培养学生分析问题、解决问题、计算的能力.

练习册系列答案
相关题目
6.下列属于合金的是( )
| A. | 生铁 | B. | 铁矿石 | C. | 四氧化三铁 | D. | 铁丝 |
3.下列物质的分类中正确的是( )
| A. | 单质:氦气、石墨、黄铜 | B. | 氧化物:干冰、海水、氧化铜 | ||
| C. | 碱:苛性钠、熟石灰、氨水 | D. | 有机物:乙醇、蛋白质、碳酸钙 |
1.某物质的分子模型如图所示,下列说法错误的是( )
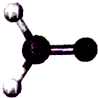

| A. | 该物质属于有机物 | B. | 该物质的化学为CH2O | ||
| C. | 该物质的1个分子中含4个原子 | D. | 氢元素的质量分数=1/30×100% |
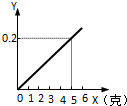 某不纯的铁粉与稀硫酸反应时,质量关系如图所示,x表示不纯铁粉消耗的质量,Y表示生成氢气的质量,试判断不纯铁粉中混入的杂质是( )
某不纯的铁粉与稀硫酸反应时,质量关系如图所示,x表示不纯铁粉消耗的质量,Y表示生成氢气的质量,试判断不纯铁粉中混入的杂质是( )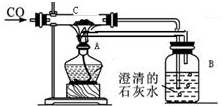 有位同学设计了下列实验(装置及所用药品如图所示),仔细观察后回答下列问题.
有位同学设计了下列实验(装置及所用药品如图所示),仔细观察后回答下列问题.