题目内容
2.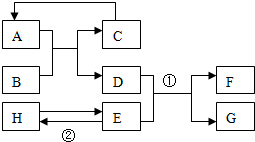 已知A-H均为初中化学常见的物质,其中A、C是组成元素相同的气体,且C能产生温室效应:是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据如图所示的转化关系(图中反应条件均已略去),请回答:
已知A-H均为初中化学常见的物质,其中A、C是组成元素相同的气体,且C能产生温室效应:是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据如图所示的转化关系(图中反应条件均已略去),请回答:(1)C的化学式:CO2.
(2)写出一个符合反应②的化学方程式CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
(3)我国工业制硫酸的第一步反应是换铁矿(主要成分为FeS2)即FeS2与氧气在高温条件下反应生成B和二氧化硫,写出该反应的化学方程式FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2.
分析 根据题目中的突破口C能产生温室效应”,所以C是二氧化碳,A、C是组成元素相同的气体,所以A是一氧化碳,“B为红棕色,是赤铁矿的主要成分”、所以B是氧化铁,“F是紫红色金属,故F是铜;H是蓝色沉淀”,H是氢氧化铜沉淀,再进一步进行分析即可.
解答 解:C能产生温室效应”,所以C是二氧化碳,A、C是组成元素相同的气体,所以A是一氧化碳,“B为红棕色,是赤铁矿的主要成分”、所以B是氧化铁,一氧化碳还原氧化铁生成二氧化碳和铁,故C是二氧化碳,D为铁,H是蓝色沉淀”,故H是氢氧化铜沉淀,“F是紫红色金属,故F是铜;D与E反应产生铜,故E为铜盐溶液,由E铜盐溶液制取氢氧化铜可跟碱溶液反应.
(1)由上述分析可知C是二氧化碳,化学式是CO2;
(2)由上述分析可知D为铁,E为铜盐溶液,铜盐溶液与碱反应可制取氢氧化铜沉淀,反应的化学方程式为
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(3)硫铁矿主要含FeS,在高温下,将硫铁矿的粉末与氧气充分反应生成三氧化二铁和二氧化硫,反应的化学方程式为:FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2.
故答案为:
(1)CO2;(2)CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(3)FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2.
点评 解答本题关键是要找出突破口,知道造成温室效应的主要气体是二氧化碳,赤铁矿的主要成分是氧化铁,紫色金属是铜,蓝色沉淀是氢氧化铜,再根据学过去的知识进一步进行分析推断即可.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
12.下列有关水的说法正确的是( )
| A. | 净化水的方法有吸附、沉降、过滤和蒸发等 | |
| B. | 水通电分解产生的正极和负极的气体体积比为2:1 | |
| C. | 为了增强水的导电性在电解水实验中需加入少量氯化钠 | |
| D. | 为了防止水结冰可在汽车水箱中加入少量乙二醇 |
10.黎老师在课堂上给同学们出了一道计算题,让同学们练习.题目如下:
扣扣同学用锌和稀硫酸制取氢气,他向发生装置中加入一定量锌粒,将30g稀硫酸分三次加入,每次产生气体的质量如下表.
(1)共制得氢气多少克?
(2)试计算所用稀硫酸的溶质质量分数为多少.
黎老师收集同学们的练习发现,第一小题的答案,全班没有异议;第二小题的答案,全班出现两种结果,①16.3%和②19.6%.你需要回答的问题是:
(1)共制得氢气0.1g.
(2)第二小题你同意的结果是②(填序号).
(3)写出第二小题的完整计算过程.
扣扣同学用锌和稀硫酸制取氢气,他向发生装置中加入一定量锌粒,将30g稀硫酸分三次加入,每次产生气体的质量如下表.
| 次数 | 第一次 | 第二次 | 第三次 |
| 加入稀硫酸质量/g | 10 | 10 | 10 |
| 生成氢气质量/g | 0.04 | 0.04 | 0.02 |
(2)试计算所用稀硫酸的溶质质量分数为多少.
黎老师收集同学们的练习发现,第一小题的答案,全班没有异议;第二小题的答案,全班出现两种结果,①16.3%和②19.6%.你需要回答的问题是:
(1)共制得氢气0.1g.
(2)第二小题你同意的结果是②(填序号).
(3)写出第二小题的完整计算过程.
17.下列说法正确的是( )
| A. | 3g碳在100g氧气中充分燃烧生成103g二氧化碳 | |
| B. | 100mL98%的浓硫酸用100mL水稀释,可得到溶质质量分数为49%的硫酸 | |
| C. | 用含杂质(杂质不与酸反应,也不溶于水)的铁10g 和50g 稀硫酸完全反应后,滤去杂质,所得液体质量为55.4g,则含杂质的铁中铁的质量分数为56% | |
| D. | MgO与CuO的混合物与98g10%的稀硫酸恰好完全反应,则原混合物中氧元素的质量是1.6g |
7.将一定质量的铁粉加至H2SO4、MgSO4和CuSO4的混合溶液中,充分反应后过滤,得到滤液M和滤渣N.下列有关说法中,合理的是( )
| A. | 滤液M中可能存在Fe2+ | |
| B. | 滤液M中一定含有两种金属阳离子 | |
| C. | 滤渣N中一定没有单质镁 | |
| D. | 滤渣N的质量一定大于加入铁粉的质量 |
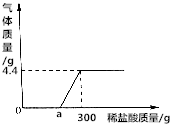 取24.8gCaCO3和Ca(OH)2固体混合物于烧杯中,向烧杯中不断加入质量分数为7.3%的稀盐酸.反应过程中测得生成气体的质量与所加稀盐酸质量的关系如图所示.
取24.8gCaCO3和Ca(OH)2固体混合物于烧杯中,向烧杯中不断加入质量分数为7.3%的稀盐酸.反应过程中测得生成气体的质量与所加稀盐酸质量的关系如图所示.