题目内容
12.化学兴趣小组的同学对“二氧化锰在过氧化氢分解前后的质量和化学性质没有改变”这一结论产生了兴趣,决定进行验证.【查阅资料】(催化剂)在化学反应中能改变其他物质的化学速率,而本身的质量和化学性质不发生改变.
【初步验证】小华提出先用电子天平称量1.0g的二氧化锰,然后让其与过氧化氢溶液反应,请写出该反应的化学方程式2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,待反应结束后,过滤,再进行二次称量,结果发现所得数据大于1.0g,原因可能是过滤后二氧化锰可能带有一定量的水分.
【实验改进】小强针对上述原因,提出烘干后再称量的方案,结果得到了准确的实验结论,与此同时,老师引导同学们可以尝试蒸发的方法,结果也得到了相同的结果.蒸发过程中用玻璃棒不断搅拌的目的是受热均匀,防止液滴飞溅.
【深入探究】对于二氧化锰在反应前后化学性质没有改变的验证,小兵提出可以直接向蒸干后的二氧化锰中滴入过氧化氢溶液,若能观察到仍有有大量气泡产生的现象,就可以得出结论.但小芳对此产生了异议,她的理由是没有催化剂过氧化氢也能分解.
【反思交流】上述实验验证的过程主要用到了定量分析的方法,这在化学知识的学习中并不陌生.请你举出定量分析方法的另一处具体运用质量守恒定律的测定.
分析 根据过氧化氢在二氧化锰的催化作用下生成水和氧气进行分析;
根据蒸发过程中玻璃棒不断搅拌的目的是受热均匀,防止液滴飞溅进行分析;
根据小兵同学的实验是想证明二氧化锰的性质在反应前后不变,因此看到的现象应是有大量气泡产生,带火星的木条复燃,常温下,没有催化剂过氧化氢也能分解;
根据定量分析的应用进行分析.
解答 解:过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
过滤后二氧化锰可能带有一定量的水分,所以质量会增大,故填:过滤后二氧化锰可能带有一定量的水分;蒸发过程中玻璃棒不断搅拌的目的是受热均匀,防止液滴飞溅,故填:受热均匀,防止液滴飞溅;
小兵同学的实验是想证明二氧化锰的性质在反应前后不变,因此看到的现象有大量气泡产生,故填:有大量气泡产生;
常温下,没有催化剂过氧化氢也能分解,只是分解较慢,只看到有气泡生成,不能证明二氧化锰的催化作用,要有对比实验,故填:没有催化剂过氧化氢也能分解;
定量分析可用于多种实验,比如质量守恒定律的测定,故填:质量守恒定律的测定.
点评 本题主要考查了催化剂和催化作用,以及化学方程式的书写、蒸发等,难度不大.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案
相关题目
3.食品安全至关重要.下列做法符合食品安全要求的是( )
| A. | 用甲醛溶液浸泡海产品保鲜 | |
| B. | 食用“加碘食盐”,可预防甲状腺肿大 | |
| C. | 用地沟油精制食用油,可节约成本 | |
| D. | 食品中添加大量防腐剂以延长其保质期 |
20. 弄清事物的原因才能找到解决办法,掌握燃烧的条件就能学会灭火的方法.结合图示将下列灭火事例进行分类.
弄清事物的原因才能找到解决办法,掌握燃烧的条件就能学会灭火的方法.结合图示将下列灭火事例进行分类.
a.釜底抽薪 b.吹灭蜡烛 c.用沙土灭火
d.用高压水枪对楼房灭火 e.关闭炉灶阀门熄火
 弄清事物的原因才能找到解决办法,掌握燃烧的条件就能学会灭火的方法.结合图示将下列灭火事例进行分类.
弄清事物的原因才能找到解决办法,掌握燃烧的条件就能学会灭火的方法.结合图示将下列灭火事例进行分类.a.釜底抽薪 b.吹灭蜡烛 c.用沙土灭火
d.用高压水枪对楼房灭火 e.关闭炉灶阀门熄火
| 主要灭火原理 | 相应的事例(填字母) |
| A.隔绝氧气 | c |
| B.清除可燃物 | ae |
| C.降低可燃物的温度至着火点以下 | bd |
4.化学活动小组同学为探究某赤铁矿石样品的纯度,先后进行了三次实验,实验数据如表:
根据上述实验数据,试回答下列问题:(赤铁矿石样品中所含杂质不与其它任何物质反应也不溶于水)
(1)实验中发生反应的化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(2)此赤铁矿石样品的纯度为:80%;
(3)根据已知条件列出求解第三次实验中稀硫酸中参加反应的硫酸质量(X)的比例式:
(4)如果用98%的浓硫酸配制第二次实验所用的稀硫酸,需加水的质量为:370g;
(5)将第三次实验后烧杯内物质过滤,向所得的不饱和溶液中加入84g的水后,则所得溶液的溶质质量分数为9.6%;
(6)如果将第三次实验中的剩余固体经过洗涤,干燥,并用足量的一氧化碳进行还原,则最终可得到固体的质量为11g.
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 所取赤铁矿石样品的质量/g | 20 | 20 | 30 |
| 所加稀硫酸的质量/g | 500 | 400 | 300 |
| 烧杯内剩余固体的质量/g | 4 | 4 | 14 |
(1)实验中发生反应的化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(2)此赤铁矿石样品的纯度为:80%;
(3)根据已知条件列出求解第三次实验中稀硫酸中参加反应的硫酸质量(X)的比例式:
(4)如果用98%的浓硫酸配制第二次实验所用的稀硫酸,需加水的质量为:370g;
(5)将第三次实验后烧杯内物质过滤,向所得的不饱和溶液中加入84g的水后,则所得溶液的溶质质量分数为9.6%;
(6)如果将第三次实验中的剩余固体经过洗涤,干燥,并用足量的一氧化碳进行还原,则最终可得到固体的质量为11g.
1.下列说法正确的是( )
| A. | 金刚石与石墨物理性质差异较大,是由于碳原子的结构不同 | |
| B. | 盐酸与硫酸化学性质相似,是由于在水溶液中都解离出H+ | |
| C. | 在化学反应中有新物质生成,是由于反应中分子和原子的种类都发生了变化 | |
| D. | “干冰升华”是由于分子本身的体积急剧增大 |
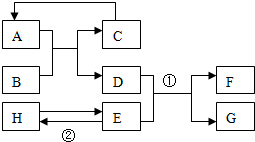 已知A-H均为初中化学常见的物质,其中A、C是组成元素相同的气体,且C能产生温室效应:是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据如图所示的转化关系(图中反应条件均已略去),请回答:
已知A-H均为初中化学常见的物质,其中A、C是组成元素相同的气体,且C能产生温室效应:是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据如图所示的转化关系(图中反应条件均已略去),请回答: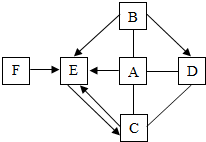 A、B、C、D、E、F为初中化学常见物质,A、B两溶液发生中和反应,固体C常用于改良酸性土壤,且C和D反应可制得B;E、F的物质类别相同,且F能与A溶液发生反应,已知上述物质间存在如图所示的关系(“→”表示转化关系,“-”表示反应关系).
A、B、C、D、E、F为初中化学常见物质,A、B两溶液发生中和反应,固体C常用于改良酸性土壤,且C和D反应可制得B;E、F的物质类别相同,且F能与A溶液发生反应,已知上述物质间存在如图所示的关系(“→”表示转化关系,“-”表示反应关系). A、B、C、D、E是初中化学课本中常涉及到的五种不同类别的物质,A为单质,C在农业上常用来改良酸性土壤,D在工业上可以除铁锈,请你仔细阅读和思考后回答下列有关问题:
A、B、C、D、E是初中化学课本中常涉及到的五种不同类别的物质,A为单质,C在农业上常用来改良酸性土壤,D在工业上可以除铁锈,请你仔细阅读和思考后回答下列有关问题: