题目内容
2.为了测定硫酸铜晶体(CuSO4•5H2O)中的结晶水的含量,做下列实验,将硫酸铜晶体放在坩埚里加热,至质量不再变化为止,测得数据见表回答:| 物质 | 质量(克) |
| 坩埚+硫酸铜晶体 | 45.5 |
| 坩埚+无水硫酸铜 | 35.5 |
| 坩埚 | 20.5 |
(2)硫酸铜晶体中结晶水的质量分数为40%.
(3)比较结晶水含量的实验值和理论值,偏差的原因是加热过程中有少量晶体溅出(填一点).
分析 (1)根据反应的特点分析;
(2)根据实验数据分析;
(3)根据实验数据与理论值对比分析.
解答 解:(1)该反应为硫酸铜晶体受热分解为硫酸铜和水,符合“一变多”特点,属于分解反应;
(2)硫酸铜晶体中结晶水的质量分数为$\frac{45.5g-35.5g}{45.5g-20.5g}$×100%=40%;
(3)结晶水含量的实验值为40%然而理论上硫酸铜晶体中结晶水的质量分数为$\frac{90}{250}$×100%=36%,加热过程中有少量晶体溅出;实验前,晶体表面潮湿,加热后水挥发等,导致水的质量测定结果偏大.
故答案为:(1)分解反应
(2)40%;
(3)加热过程中有少量晶体溅出(或实验前,晶体表面潮湿,加热后水挥发等).
点评 本题是一道定量实验题,既要学生分析实验的关键、细节,又要求对实验结果产生的误差的原因进行分析.

练习册系列答案
相关题目
11.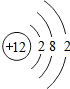 如图是某原子的结构示意图.下列说法不正确的是( )
如图是某原子的结构示意图.下列说法不正确的是( )
 如图是某原子的结构示意图.下列说法不正确的是( )
如图是某原子的结构示意图.下列说法不正确的是( )| A. | 该原子的质子数为12 | B. | 如图表示的是金属原子 | ||
| C. | 该原子的核外电子数为12 | D. | 该原子的化学性质与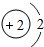 化学性质相似 化学性质相似 |
12.下列有关空气的说法正确的是( )
| A. | 空气中含量最多的是氮气 | |
| B. | 空气是由氧气和氮气组成,其中氧气的质量约占空气质量的$\frac{1}{5}$ | |
| C. | 空气中二氧化碳的体积只占0.03%,因此它的作用很小 | |
| D. | 空气质量报告中所列的空气质量级别数目越大,空气质量越好 |