题目内容
7. 根据如图回答问题:
根据如图回答问题:(1)写出图中标号仪器名称:①长颈漏斗;
(2)实验室用氯酸钾制取并收集纯净的氧气应选用的装置是AF(填序号,下同).反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)常温下块状电石(CaC2)与水反应生成乙炔(C2H2)气体和氧化钙,该反应的化学方程式是CaC2+2H2O=Ca(OH)2+C2H2↑,实验室制取乙炔时,须严格控制加水速度,以免剧烈反应放热引起装置炸裂.图中适合制取乙炔气体的发生装置有C;
(4)实验室制取CO2的实验结束后,从反应残留物中提取固体溶质时,按如下流程操作:
 ,过滤所用的玻璃仪器除烧杯、漏斗外,还有玻璃棒(填仪器名称),在蒸发过程中,当蒸发皿中出现较多量固体时,停止加热,利用蒸发皿的余热使滤液蒸干.
,过滤所用的玻璃仪器除烧杯、漏斗外,还有玻璃棒(填仪器名称),在蒸发过程中,当蒸发皿中出现较多量固体时,停止加热,利用蒸发皿的余热使滤液蒸干.
分析 长颈漏斗方便加液体药品,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,用排水法收集的氧气更纯净.常温下块状电石(CaC2)与水反应生成乙炔(C2H2)气体和氧化钙,配平即可;实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.过滤所用的玻璃仪器除烧杯、漏斗外,还有玻璃棒;在蒸发过程中,当蒸发皿中出现较多量固体时,停止加热,利用蒸发皿的余热使滤液蒸干.
解答 解:(1)长颈漏斗方便加液体药品,故答案为:长颈漏斗;
(2)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,用排水法收集的氧气更纯净;故答案为:AF;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(3)常温下块状电石(CaC2)与水反应生成乙炔(C2H2)气体和氧化钙,配平即可;实验室制取乙炔时,须严格控制加水速度,以免剧烈反应放热引起装置炸裂.图中适合制取乙炔气体的发生装置有C,因为注射器可以控制反应的速率,故答案为:CaC2+2H2O=Ca(OH)2+C2H2↑;C;
(4)过滤所用的玻璃仪器除烧杯、漏斗外,还有玻璃棒;在蒸发过程中,当蒸发皿中出现较多量固体时,停止加热,利用蒸发皿的余热使滤液蒸干;故答案为:玻璃棒;蒸发皿中出现较多量固体;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、过滤和蒸发等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 金刚石的硬度大,可用于切割玻璃 | |
| B. | 聚乙烯塑料有热塑性,可用于食品袋加热封口 | |
| C. | 锡铅合金熔点低,可用于焊接金属 | |
| D. | 铝的化学性质稳定,可在铁栏杆的表面涂铝粉防止生锈 |
| A. | 一个单宁酸分子中含26个氢分子 | |
| B. | 单宁酸中氧元素的质量分数最低 | |
| C. | 单宁酸分子中碳、氢、氧元素质量比为38:26:23 | |
| D. | 一个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成 |
| A. |  服用胃舒平[主要成分是Al(OH)3]治疗胃酸过多,胃液pH的变化 | |
| B. |  向一定质量的稀盐酸和氯化铜的混合溶液中加入氢氧化钠溶液 | |
| C. |  将等质量的镁和铁分别投入到盛有足量同种稀硫酸的两个容器中 | |
| D. |  浓盐酸敞口放置 |




 如图所示为A、B、C三种固体物质的溶解度曲线,下列有关说法正确的是B.
如图所示为A、B、C三种固体物质的溶解度曲线,下列有关说法正确的是B.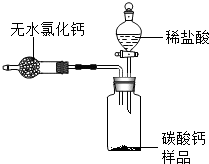 为测定某市售碳酸钙药品中碳酸钙的质量分数(杂质为SiO2,与稀盐酸不反应),某同学设计了如下实验方案(已知:无水氯化钙是常见的干燥剂):
为测定某市售碳酸钙药品中碳酸钙的质量分数(杂质为SiO2,与稀盐酸不反应),某同学设计了如下实验方案(已知:无水氯化钙是常见的干燥剂): 学习小组进行了如图所示的实验,分别试验了图中四种液体的导电性.
学习小组进行了如图所示的实验,分别试验了图中四种液体的导电性.