题目内容
4.下列除去物质中所含杂质(括号内的物质)的方法错误的是( )| A. | CO2(HCl)--通入足量的氢氧化钠溶液,干燥 | |
| B. | NaCl(泥沙)--加入足量的水溶解、过滤、蒸发 | |
| C. | K2SO4(K2CO3)--加入足量的稀盐酸,蒸发 | |
| D. | O2(H2O)--通入足量的浓硫酸中 |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、氯化钠易溶于水,泥沙难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故选项所采取的方法正确.
C、K2CO3能与稀盐酸反应生成氯化钾、水和二氧化碳,能除去杂质但引入了新的杂质氯化钾,不符合除杂原则,故选项所采取的方法错误.
D、浓硫酸具有吸水性,且不与O2反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:AC.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
16.实验探究:比较凌晨森林公园的空气中二氧化碳和氧气的含量与日照后森林公园的空气中二氧化碳和氧气的含量.
| 比较项目 | 实验操作 | 实验现象 | 得出结论 |
| 二氧化碳的含量 | 将澄清石灰水分别滴入盛有凌晨的空气和日照后的空气的集气瓶中 | 凌晨的空气变浑浊,日照后的空气中现象不明显 | 凌晨的空气中二氧化碳的含量比日照后的空气中更 高 |
| 氧气的含量 | 将燃着的木条分别伸入盛有凌晨的空气和日照后的空气你的集气瓶中 | 凌晨的空气中的木条很快熄灭,日照后的空气中的木条能燃烧一会再熄灭 | 凌晨的空气中氧气的含量比日照后的空气中更低 |
9.含硫化氢(H2S)的工业废气排入空气会造成污染.可采用NaOH溶液进行吸收,同时可以制得某种可溶性化合物Y,反应的化学方程式为H2S+2NaOH=Y+2H2O,工艺流程图如下图所示:

下列说法正确的是( )

下列说法正确的是( )
| A. | 硫化氢溶液的酸碱度可用石蕊试液测定 | |
| B. | “系列操作”中一定有过滤的操作 | |
| C. | Y的化学式为Na2SO4 | |
| D. | 吸收H2S的反应是中和反应 |
16.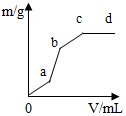 向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入溶液的体积V之间的关系如图所示,关于该曲线的推测正确的是( )
向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入溶液的体积V之间的关系如图所示,关于该曲线的推测正确的是( )
 向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入溶液的体积V之间的关系如图所示,关于该曲线的推测正确的是( )
向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入溶液的体积V之间的关系如图所示,关于该曲线的推测正确的是( )| A. | a-b产生的沉淀为硫酸钡 | |
| B. | a-b产生的沉淀为氢氧化镁 | |
| C. | b-c产生的沉淀为硫酸钡和氢氧化镁 | |
| D. | b-c产生的沉淀为氢氧化镁 |
13.下列试剂瓶标签上的化学式书写错误的是( )
| A. |  | B. |  | C. |  | D. |  |
14.区分下列常见的各组物质时,所用方法错误的是( )
| A. | 氯化钠与硝酸铵固体--加蒸馏水溶解 | |
| B. | 羊毛和棉织品--燃烧闻气味 | |
| C. | 一氧化碳和甲烷--点燃,观察火焰颜色 | |
| D. | 铜片和铁块--观察颜色 |