题目内容
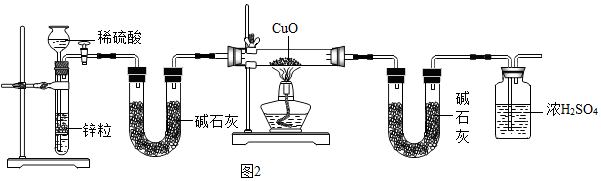
19.探究学习小组在实验室中用图1所示装置制取CO2并探究CO2与过氧化钠(Na2O2)的反应.查阅资料得知:过氧化钠(Na2O2)是一种淡黄色固体,能与CO2,H2O发生反应:Na2O2+2CO2═2Na2CO3+O2,2Na2O2+H2O═4NaOH+O2↑
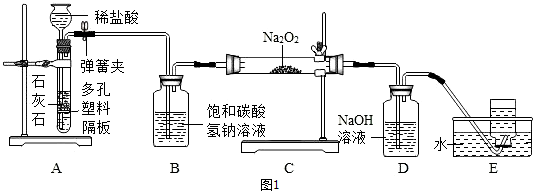
请回答下列问题:(1)利用装置A制取CO2的优点是便于控制反应的发生和停止.
(2)装置B的作用是吸收CO2中混有的HCl,发生反应的化学方程式为NaHCO3+HCl=NaCl+H2O+CO2↑.
(3)装置D的作用是除去二氧化碳气体.
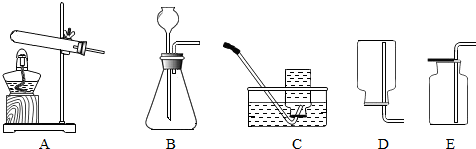
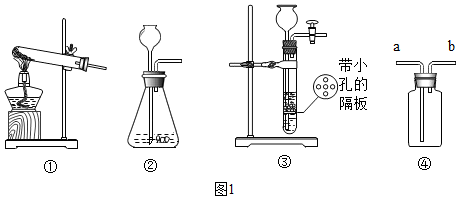
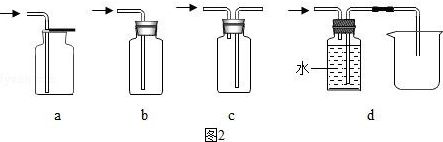
(4)装置E中收集到的气体是O2(填化学式),该气体还可以用下列图2装置中的a、d进行收集(填写字母序号).
(5)为探究反应后装置C硬质玻璃管中固体的成分,该小组同学进行了如图3实验:
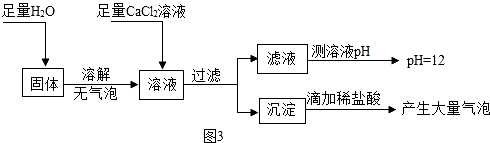
根据判断,反应后装置C硬质玻璃管中固体为氢氧化钠和碳酸钠.
分析 (1)根据装置A可以通过压强的作用是固体和液体分离进行分析;
(2)根据碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳进行分析;
(3)根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析;
(4)根据过氧化钠和二氧化碳、水反应会生成氧气,氢氧化钠可以将二氧化碳除去进行分析;
(5)根据过氧化钠和水会生成氧气,碳酸钠和氯化钙会生成碳酸钙沉淀,碳酸钙和盐酸反应会生成二氧化碳气体,氢氧化钠溶液显碱性进行分析.
解答 解:(1)装置A可以通过压强的作用是固体和液体分离,所以利用装置A制取CO2的优点是:便于控制反应的发生和停止;
(2)碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑;
(3)氢氧化钠和二氧化碳反应生成碳酸钠和水,所以装置D的作用是除去二氧化碳气体;
(4)过氧化钠和二氧化碳、水反应会生成氧气,氢氧化钠可以将二氧化碳除去,所以装置E中收集到的气体是O2,氧气密度比空气大,不易溶于水,密度比水小,所以还可以用下列图2装置中的a、d进行收集;
(5)过氧化钠和水会生成氧气,碳酸钠和氯化钙会生成碳酸钙沉淀,碳酸钙和盐酸反应会生成二氧化碳气体,氢氧化钠溶液显碱性.
固体加水没有气泡,所以不含过氧化钠,加入氯化钙会生成白色沉淀,白色沉淀加盐酸,会生成气体,所以含有碳酸钠,反应后滤液的pH值是12,所以含有氢氧化钠,
所以反应后装置C硬质玻璃管中固体为氢氧化钠和碳酸钠.
故答案为:(1)便于控制反应的发生和停止;
(2)NaHCO3+HCl=NaCl+H2O+CO2↑;
(3)除去二氧化碳气体;
(4)O2,a、d;
(5)氢氧化钠和碳酸钠.
点评 解答此题的关键是根据反应物的类型及反应条件正确选择装置,正确进行知识的类比和前后联系,熟知典型的化学方程式的书写.

 阅读快车系列答案
阅读快车系列答案| A. | CO2(HCl)--通入足量的氢氧化钠溶液,干燥 | |
| B. | NaCl(泥沙)--加入足量的水溶解、过滤、蒸发 | |
| C. | K2SO4(K2CO3)--加入足量的稀盐酸,蒸发 | |
| D. | O2(H2O)--通入足量的浓硫酸中 |
实验一、探究二氧化碳与水的反应(取四朵用紫色石蕊溶液染成紫色的干燥的小花,进行如图所示实验)

实验现象:(I)、(IV)中的小花变红.
设计(Ⅱ)、(Ⅲ)实验的目的是:验证水和二氧化碳分别是否能使紫色石蕊变色.
该实验的探究方法是:设计分析B(填“A”或“B”或“C”,获得结论.
A.仅一个单因素的实验
B.有多种因素的对比实验
C.用前面实验的生成物继续实验
实验二、验证二氧化碳与氢氧化钠溶液也发生了反应
我们知道,二氧化碳能使澄清石灰水发生反应生成碳酸钙而变浑浊.彩云同学查阅资料发现:氢氧化钠与氢氧化钙化学性质十分相似,也能与二氧化碳发生反应,但此反应无明显实验现象,其反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O.她为了能证明氢氧化钠与二氧化碳在溶液中确实发生了反应,设计了如下方案.请你将她设计的方案补充完整:
| 实验步骤和方法 | 实验现象 | 实验结论 | 启示 | |
| 方案1 | 向一个软塑料瓶中充满二氧化碳,再注入少量氢氧化钠溶液,盖紧瓶盖,摇动塑料瓶. | 塑料瓶变瘪 | CO2与NaOH发生了化学反应 | 从反应物二氧化碳的减少(压强减小)来判断反应的发生 |
| 方案2 | 向充满CO2气体的集气瓶中倒入适量的NaOH溶液振荡,再向其中加入适量的稀盐酸 | 有气泡冒出 | CO2与NaOH发生了化学反应 | 从生成物的存在来判断反应的发生 |