题目内容
6.“侯氏制碱法”制得的纯碱(Na2CO3)中常含有少量氯化钠.某化学兴趣小组的同学拟测定某纯碱样品中Na2CO3的质量分数.称取该纯碱样品10g,加入到盛有50g的稀盐酸的烧杯中,恰好完全反应,使气体全部放出,得到氯化钠溶液的质量为56.7g.请你计算:
(1)反应中产生的CO2的质量是3.3g.
(2)求该纯碱样品中Na2CO3的质量分数.(写出具体计算过程)
分析 向混有氯化钠的纯碱中滴加盐酸,氯化钠不与盐酸反应而碳酸钠与盐酸反应生成氯化钠、水和气体二氧化碳;根据质量守恒定律求出反应中放出二氧化碳的质量,利用反应的化学方程式可计算出混合物中碳酸钠的质量;进而求得纯碱中Na2CO3的质量分数.
解答 解:(1)根据质量守恒定律,反应生成的二氧化碳的质量是:10g+50g-56.7g=3.3g;
(2)设纯碱中Na2CO3的质量为x.
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 44
x 3.3g
$\frac{106}{x}=\frac{44}{3.3g}$
x=7.95g
纯碱中Na2CO3的质量分数:$\frac{7.95g}{10g}$×100%=79.5%
答:(1)产生CO2的质量3.3 g;
(2)纯碱中Na2CO3的质量分数为79.5%.
点评 根据化学方程式可以表示反应中各物质的质量比,由反应中任意物质的质量可计算出反应中其它物质的质量.

练习册系列答案
相关题目
8.下列燃料,对环境最友好的是( )
| A. | 煤 | B. | 氢气 | C. | 汽油 | D. | 天然气 |
5.实验室可用如图所示装置制取少量O2,下列说法正确的是( )
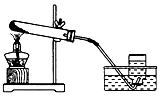

| A. | 试管中盛放的试剂是二氧化锰和双氧水 | |
| B. | 当水槽中导管口一有气泡逸出时,就立即收集O2 | |
| C. | 实验结束时先从水槽中取出导管,再撤走酒精灯 | |
| D. | 实验室还可用向下排空气法收集O2 |
11.A、B、C、D四种金属中只有C在自然界中以单质形式存在,把A、B两种金属分别放入等质量的稀盐酸中,D加入到B(NO3) 2溶液中,反应关系如图所示.据此判断下列说法中错误的是( )


| A. | A、B与酸反应产生氢气质量相等 | |
| B. | D和B(NO3)2溶液中发生了反应 | |
| C. | 四种金属的活动性顺序为A>B>D>C | |
| D. | A、B与盐酸反应中消耗的盐酸质量相等 |
18.向AgNO3溶液中加入一定质量Fe和Al,充分反应后过滤,得到滤渣和浅绿色滤液.下列说法正确的是( )
| A. | 滤渣中一定含有Fe | B. | 滤渣中一定含有Ag | ||
| C. | 滤液中一定含有Al3+、Ag+ | D. | 滤液中一定含有Fe2+、Ag+ |
15.向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入n克Zn,充分反应后过滤,将滤渣洗涤、干燥、称量,得到的质量为n克的滤渣,下列说法正确的是( )
| A. | 取滤渣滴加稀硫酸,可能有气泡产生 | |
| B. | 取反应后的滤液观察,滤液一定呈蓝色 | |
| C. | 取反应后的滤液滴加稀盐酸,有白色沉淀产生 | |
| D. | 滤液中的溶质最多有两种,滤渣中的物质至少有两种 |
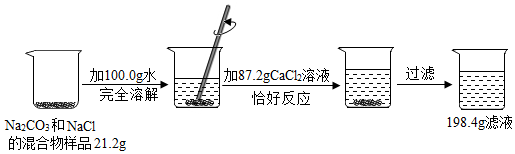

 表示的粒子是Al3+.
表示的粒子是Al3+.