题目内容
11.A、B、C、D四种金属中只有C在自然界中以单质形式存在,把A、B两种金属分别放入等质量的稀盐酸中,D加入到B(NO3) 2溶液中,反应关系如图所示.据此判断下列说法中错误的是( )
| A. | A、B与酸反应产生氢气质量相等 | |
| B. | D和B(NO3)2溶液中发生了反应 | |
| C. | 四种金属的活动性顺序为A>B>D>C | |
| D. | A、B与盐酸反应中消耗的盐酸质量相等 |
分析 金属越活泼,和酸反应的速率越快,相同条件下反应需要的时间越短;
四种金属中只有C在自然界中以单质形式存在,说明C最不活泼;
金属和酸反应时,产生的氢气中的氢元素完全来自于酸,即产生氢气的质量决定于反应的酸的质量.
解答 解:A、由图1可知,A、B与酸反应产生氢气质量相等,该选项说法正确;
B、由图2可知,D加入到B(NO3) 2溶液中,溶液质量不变,说明D不能和B(NO3) 2反应,即B比D活泼,该选项说法不正确;
C、由图1可知,A比B活泼,由图2可知,B比D活泼,C最不活泼,因此四种金属的活动性顺序为A>B>D>C,该选项说法正确;
D、由图1可知,A、B与酸反应产生氢气质量相等,因此A、B与盐酸反应中消耗的盐酸质量相等,该选项说法正确.
故选:B.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
13. 已知氯化钠和硝酸钾的溶解度如表:
已知氯化钠和硝酸钾的溶解度如表:
(1)20℃时,氯化钠饱和溶液的溶质质量分数是26.5%.
(2)请在如图中画出KNO3的溶解度曲线:图中两溶解度曲线交点的意义是在该温度下,氯化钠和硝酸钾的溶解度相等.
(3)KNO3是化学肥料中的复合肥料,从热的KNO3浓溶液中析出晶体的方法是降温结晶或冷却.
 已知氯化钠和硝酸钾的溶解度如表:
已知氯化钠和硝酸钾的溶解度如表:| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | |
(2)请在如图中画出KNO3的溶解度曲线:图中两溶解度曲线交点的意义是在该温度下,氯化钠和硝酸钾的溶解度相等.
(3)KNO3是化学肥料中的复合肥料,从热的KNO3浓溶液中析出晶体的方法是降温结晶或冷却.
10.通过下列实验,能达到实验目的是( )

| A. | 通过观察甲装置小试管中产生气泡的速率,比较MnO2和CuO的催化效果 | |
| B. | 通过观察乙装置试管中溶液颜色深浅,比较盐酸和碳酸的酸性强弱 | |
| C. | 通过观察丙装置气球的大小变化,比较NaOH和NH4NO3固体溶解的热效应 | |
| D. | 通过观察丁装置干燥的烧杯壁是否出现水滴,判断点燃的气体是甲烷还是氢气 |
16.向一定量的AgNO3与Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤,分析判断下列说法正确的是( )
| A. | 滤渣中一定有Zn,可能有Ag | |
| B. | 滤渣中一定有Cu、Ag,可能有Zn | |
| C. | 滤液中只有Zn(NO3)2 | |
| D. | 滤液中一定有Zn(NO3)2,可能有Cu(NO3)2和AgNO3 |
20.下列实验方案设计不合理的是( )
| 选项 | 实验内容 | 操作或所用试剂 |
| A | 鉴别硬水和软水 | 加肥皂水 |
| B | 鉴别硫酸铵和硫酸钾 | 加熟石灰,混合研磨 |
| C | 除去CO2中混有的HCl | 通入足量的NaOH溶液 |
| D | 除去氯化钾中的二氧化锰 | 加水溶解、过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
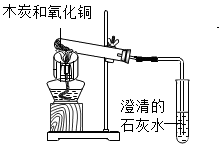 木炭还原氧化铜的实验装置如图所示
木炭还原氧化铜的实验装置如图所示