题目内容
7.已知:Na2CO3+CaCl2=CaCO3+2NaCl.根据图9所示的实验过程和提供的,计算该样品中Na2CO3 的质量分数.(写出计算过程)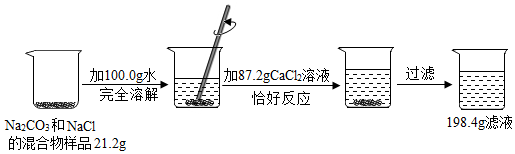
分析 根据图中所给的数据结合质量守恒定律可以求出生成的碳酸钙的质量,然后可以根据沉淀的质量求出碳酸钠的质量,进而求出该样品中Na2CO3 的质量分数.
解答 解:由质量守恒定律结合题给的数据可以知道生成碳酸钙的质量为:21.2g+100.0g+87.2g-198.4g=10g;
设混合物中碳酸钠的质量为x
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 10g
$\frac{106}{100}=\frac{x}{10g}$ 解得:x=10.6g
样品中Na2CO3 的质量分数是:$\frac{10.6g}{21.2g}×100%$=50%;
答:样品中碳酸钠的质量分数是50%.
点评 本题中考查的知识点较多,主要是依据化学方程式进行计算,在解答时要注意运用质量守恒定律来得出计算所必须的已知量,然后依据化学方程式进行计算.

练习册系列答案
相关题目
17.有四种无色溶液a、b、c、d分别是H2SO4、Na2CO3、K2SO4、Ba(NO3)2中的一种,如下实验:①a+d→溶液+气体;②b+c→溶液+沉淀;③b+d→沉淀e+溶液;④a+b→溶液f+沉淀,⑤e+f→溶液+气体.则a、b、c、d依次是( )
| A. | Na2CO3、Ba(NO3)2、K2SO4、H2SO4 | B. | K2SO4、Ba(NO3)2、Na2CO3、H2SO4 | ||
| C. | H2SO4、K2SO4、Ba(NO3)2、Na2CO3 | D. | H2SO4、Ba(NO3)2、K2SO4、Na2CO3 |
15.下列实验操作正确的是( )
| A. | 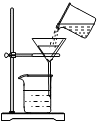 过滤 | B. | 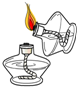 点燃酒精灯 | C. |  检查装置气密性 | D. | 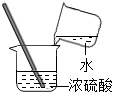 稀释浓硫酸 |
2.下列依据实验目的设计的实验方法错误的是( )
| 选项 | 实验目的 | 实验方法 |
| A | 鉴别羊毛和腈纶 | 在空气中灼烧,观察现象,闻气味 |
| B | 检验铵态氮肥 | 与碱共热,观察产生的气体能否使湿润红色 石蕊试纸变蓝色 |
| C | 除去硫酸锌溶液中少量的硫酸 | 加入过量锌粉,充分反应后过滤 |
| D | 获取纯净的氮气 | 用木炭燃烧除去空气中的氧气 |
| A. | A | B. | B | C. | C | D. | D |
16.下列依据实验目的所设计的实验操作中,正确的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 检验NaCl中含有Na2CO3 | 加水溶解 |
| B | 鉴别NaOH和Ca(OH)2溶液 | 加Na2CO3溶液 |
| C | 除去FeSO4溶液中的CuSO4 | 加适量Zn粉,过滤 |
| D | 除去CO2中的CO | 通过足量NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
 如图为两种物质在不同温度时的溶解度曲线.请回答:
如图为两种物质在不同温度时的溶解度曲线.请回答: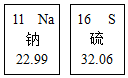 如图是两种元素在周期表中的信息.请回答:
如图是两种元素在周期表中的信息.请回答: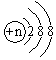 ,则n=16.
,则n=16.