题目内容
17.以下有关同位素说法错误的是( )| A. | 同种元素的各种同位素原子的化学性质基本相同,但它们的其它性质有很大差别 | |
| B. | 大多数元素都有同位素原子,氢有氕(${\;}_{1}^{1}$H)、氘(${\;}_{1}^{2}$H)、氚(${\;}_{1}^{3}$H)3 种同位素原子 | |
| C. | 互为同位素的原子,质子数和核外电子数一定相等,中子数一定不相等 | |
| D. | 金刚石和石墨都是由碳原子构成的,它们互为同位素原子 |
分析 A、元素的化学性质与原子的价电子有关;B、有相同质子数,不同中子数的原子或同一元素的不同核素互为同位素
解答 解:
A、元素的化学性质与原子的最外层电子有关,同一元素的各种同位素核外电子数相同,所以它们的化学性质相同,但物理性质不同,故A说法正确;
B、1H、2H、3H质子数相同,中子数不同,互为同位素,故B说法正确;
C、互为同位素的原子,质子数和核外电子数一定相等,中子数一定不相等,故C说法正确;
D、金刚石与石墨是由碳元素组成的物理性质不同的单质,互为同素异形体,不属于同位素,故D说法错误.
故选D.
点评 本题考查同位素的概念,难度不大.对于元素、核素、同位素、同素异形体、同分异构体、同系物、同种物质等概念的区别是考试的热点问题.

练习册系列答案
相关题目
7.下列实验设计中,能达到实验目的是( )
| A. | 将某气体点燃,在火焰上方罩上干冷烧杯,观察烧杯壁上是否有水雾--检验该气体是否为氢气 | |
| B. | 观察颜色--区分一氧化碳和二氧化碳 | |
| C. | 取样,向在空气中久置的NaOH溶液中加入过量稀盐酸--鉴别NaOH溶液是否变质 | |
| D. | 在作物的生长过程中,不施加钾肥,观察作物生长情况--探究磷对作物生长的作用 |
8.杂卤石(K2SO4•MgSO4•2CaSO4•2H2O)属于“呆矿”,为能充分利用钾资源,用饱和的Ca(OH)2溶液浸杂卤石制备硫酸钾,工艺流程如下:
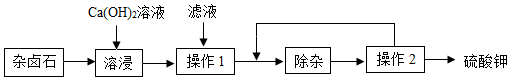
已知:
(1)操作1的名称为过滤,所需的玻璃仪器有玻璃棒、烧杯、漏斗,玻璃棒的作用是引流.
(2)滤渣的主要成分有Mg(OH)2和CaSO4.
(3)“除杂”环节中,先加入a溶液(填字母,下同),经搅拌等操作后,过滤,再加入
c溶液调滤液pH至中性.
a.K2CO3 b.Na2CO3 c.稀硫酸 d.稀盐酸
(4)操作2的步骤是蒸发浓缩、降温结晶、过滤、洗涤.
(5)洗涤硫酸钾最好选用c.
a.30℃的水 b.饱和的硫酸钠溶液 c.饱和的硫酸钾溶液.

已知:
| 物质 | CaSO4 | K2SO4 | Mg(OH)2 |
| 溶解度/g(25℃) | 0.28 | 11.1 | 0.00084 |
(2)滤渣的主要成分有Mg(OH)2和CaSO4.
(3)“除杂”环节中,先加入a溶液(填字母,下同),经搅拌等操作后,过滤,再加入
c溶液调滤液pH至中性.
a.K2CO3 b.Na2CO3 c.稀硫酸 d.稀盐酸
(4)操作2的步骤是蒸发浓缩、降温结晶、过滤、洗涤.
(5)洗涤硫酸钾最好选用c.
a.30℃的水 b.饱和的硫酸钠溶液 c.饱和的硫酸钾溶液.
5.某化学兴趣小组的同学为测定某硫酸溶液的溶质质量分数,现称取100g该硫酸溶液放于烧杯中,然后向烧杯中逐滴滴加一定溶质质量分数的氯化钡溶液至恰好完全后过滤,记录实验数据如下表所示:
(1)反应后生成硫酸钡的质量是46.6克.
(2)请计算该硫酸溶液的溶质质量分数?
| 反应前 | 反应后 | ||
| 实验数据 | 硫酸溶液质量 | 氯化钡溶液质量 | 反应后溶液质量 |
| 100克 | 100克 | 153.4克 | |
(2)请计算该硫酸溶液的溶质质量分数?
6.生活中处处有化学,下列家庭小实验中不涉及化学变化的是( )
| A. |  柠檬酸、纯碱等制汽水 | B. |  木炭除去冰箱中异味 | ||
| C. |  食醋除去水垢 | D. |  探究铁生锈的条件 |
7.物质的下列用途主要利用其物理性质的是( )
| A. | 干冰用于人工降雨 | B. | 稀盐酸用于金属表面除锈 | ||
| C. | 白醋由于清除水壶中的水垢 | D. | 苏打水用于缓解胃酸过多 |
