题目内容
3.某久置的NaOH固体中水的质量分数为3.4%,Na2CO3质量分数为10.6%,其他均为NaOH.向20g的此样品中加入过量的稀盐酸,完全反应后再加入12g10%的NaOH溶液,恰好完全中和,则所得溶液中溶质质量为29.25g.分析 氢氧化钠和稀盐酸反应生成氯化钠和水,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
反应物中的钠元素完全转化到氯化钠中;
根据提供的数据可以计算氯化钠的质量.
解答 解:设溶质氯化钠的质量为x,
氯化钠中钠元素的质量为:20g×10.6%×$\frac{46}{106}$×100%+20g×(1-3.4%-10.6%)×$\frac{23}{40}$×100%+12g×10%×$\frac{23}{40}$×100%=11.5g,
根据题意有:x×$\frac{23}{58.5}$×100%=11.5g,
x=29.25g,
故填:29.25g.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,要注意理解.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列各组物质在溶液中能大量共存且能得到无色溶液的是( )
| A. | Na2SO4、NaCl、BaCl2 | B. | H2SO4、NaCl、KNO3 | ||
| C. | CuSO4、KCl、HCl | D. | HCl、NaOH、NaCl |
14.甘谷人喜好喝罐罐茶,茶叶中含茶氨酸【化学式为C7H14O3N2】、锌、硒等多种成分,下列说法中不正确的是( )
| A. | 茶氨酸由碳、氢、氧、氮四种元素组成 | |
| B. | 茶氨酸属于有机物,锌、硒指单质 | |
| C. | 一个茶氨酸妃子中含有3个氧原子 | |
| D. | 茶氨酸中氢元素的质量分数最大 |
10.
(1)上表元素中,在地壳内含量最多的金属元素符号是Al;在人体内含量最多的元素符号是O;水中含有的+1价的元素符号是H;
(2)氯化钙的化学式CaCl2;Na2SO3中S元素的化合价为+4;
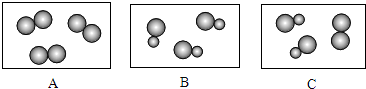
(3)如图表示气体分子示意模型,其中属于化合物的是B(填字母序号),属于混合物的是C(填字母序号).选用表中元素,表示A图中的分子,其化学式可能为H2 、O2 (或Cl2)(写出两种即可).
| 元素名称 | 钠 | 钙 | 铝 | 氢 | 氯 | 氧 | 硫 |
(2)氯化钙的化学式CaCl2;Na2SO3中S元素的化合价为+4;
(3)如图表示气体分子示意模型,其中属于化合物的是B(填字母序号),属于混合物的是C(填字母序号).选用表中元素,表示A图中的分子,其化学式可能为H2 、O2 (或Cl2)(写出两种即可).