1.碱的4条通性
①酸和各种指示剂和pH试纸反应
|
碱的名称 |
石蕊试液 |
红色石 蕊试纸 |
蓝色石 蕊试纸 |
酚酞试液 |
▲白色酚 酞试纸 |
pH试纸 |
|
氢氧化钠 |
|
|
|
|
|
|
|
氢氧化钙 |
|
|
|
|
|
|
|
*氢氧化钾 |
|
|
|
|
|
|
②酸+碱→盐+水
(注意:本反应是复分解反应[基本反应类型],且是中和反应[属于复分解反应])
|
举例 |
有关的化学方程式 |
简答 |
|
在火碱溶液中滴加硫酸溶液 |
|
反应的基本类型:
|
|
在石灰水中滴加过量的盐酸溶液 |
|
如果在此石灰水中预先滴加酚酞试液,反应后,可以看到颜色的变化是:
|
|
在氢氧化铜中滴加硫酸溶液 |
|
可以看到的实验现象是:
|
|
*在氢氧化镁中滴加硝酸溶液 |
|
可以看到的实验现象是:
|
③碱+盐→新盐+新碱
|
举例 |
有关的化学方程式 |
简答 |
|
苏打溶液和石灰水反应 |
|
反应前后,溶液的pH值 (变大、变小、不变) |
|
碳酸钾溶液和氢氧化钡溶液反应 |
|
在生成的白色沉淀中,再滴加硫酸溶液,可以看到 |
|
*硫酸铜溶液和氢氧化钾溶液反应 |
|
硫酸铜溶液是 色的。反应后,可以看到
|
|
氯化铁溶液中滴加氢氧化钠溶液 |
|
实验现象是:
|
|
*氯化镁溶液中滴加氢氧化钾溶液 |
|
在生成的白色沉淀中,再滴加硫酸溶液,可以看到 |
④碱+酸性氧化物→盐+水
|
举例 |
有关的化学方程式 |
简答 |
|
实验室用石灰水检验二氧化碳 |
|
实验现象是:
|
|
实验室用苛性钠吸收二氧化碳 |
|
反应后,得到的盐溶液的pH (<7/ =7/ <7) |
|
工业上常用氢氧化钠吸收二氧化硫 |
|
二氧化硫是一种引起 的物质 |
2.其他
①物理性质
|
名称 |
颜色 |
▲导电性 |
状态 |
挥发性 |
▲密度 |
吸水性 |
|
浓盐酸 |
无色 工业盐酸:黄 |
导电 |
液态 |
有 |
比水的密度大 |
无 |
|
硫酸 |
无色 |
无 |
浓硫酸:有 稀硫酸:无 |
|||
|
浓硝酸 |
有 |
无 |
[浓硫酸具有吸水性所以可以作为许多气体干燥剂,但是浓硫酸不能干燥氨气]
②用途
|
物质 |
用途 |
|
盐酸 |
制药、去除铁锈、制染料、味精、葡萄糖等 |
|
硫酸 |
去除铁锈、制化肥、农药和炸弹等 |
1. 酸的5条通性
①酸和各种指示剂和pH试纸反应
|
酸的名称 |
石蕊试液 |
红色石 蕊试纸 |
蓝色石 蕊试纸 |
酚酞试液 |
白色酚 酞试纸 |
pH试纸 |
|
盐酸 |
|
|
|
|
|
|
|
稀硫酸 |
|
|
|
|
|
|
|
浓硫酸 |
|
|
|
|
|
|
|
*硝酸 |
|
|
|
|
|
|
|
碳酸 |
|
|
|
|
|
|
[浓硫酸具有脱水性(化学性质),所以试纸变成黑色]
②酸+活泼金属→盐+氢气
(注意:活泼金属是指金属活动性大于氢;酸是指盐酸或者稀硫酸)
例如:请写出金属镁带、锌粒和铁钉和盐酸反应的化学方程式,并且分析为什么实验室一般选用锌粒和盐酸或者稀硫酸反应来制取氢气?
反应方程式:镁带和稀硫酸
锌粒和盐酸
铁钉和盐酸
为什么实验室一般用锌粒,而不用铁或者是镁来制取氢气?
③酸+碱→盐+水
(注意:本反应是复分解反应[基本反应类型],且是中和反应[属于复分解反应])
|
举例 |
有关的化学方程式 |
简答 |
|
在烧碱溶液中滴加盐酸溶液 |
|
反应的基本类型:
|
|
在石灰水中滴加过量的硫酸溶液 |
|
如果在石灰水中预先滴加石蕊试液,可以看到颜色的变化是: |
|
*在氢氧化铜中滴加硝酸溶液 |
|
可以看到的实验现象是:
|
|
*在氢氧化铁中滴加硝酸溶液 |
|
可以看到的实验现象是:
|
④酸+盐→新盐+新酸
|
举例 |
有关的化学方程式 |
简答 |
|
实验室制 取二氧化碳 |
|
反应的基本类型:
|
|
用氯化钡检验盐酸溶液和硫酸溶液 |
|
实验现象是: |
|
在硝酸银溶液中滴加盐酸 |
|
可以看到的实验现象是有白色沉淀,在滴加 沉淀不消失 |
|
在碳酸钠溶液中滴加盐酸溶液 |
|
可以看到的实验现象是:
|
|
在碳酸钡溶液中滴加硫酸溶液 |
|
可以看到的实验现象是:
|
⑤酸+碱性氧化物→盐+水
|
举例 |
有关的化学方程式 |
简答 |
|
用浓盐酸来 去除铁锈 |
|
实验现象:
|
|
用硫酸去 除氧化铁 |
|
反应前后铁元素的化合价 (变/不变) |
|
在黑色氧化铜粉末中滴加硫酸 |
|
实验现象是
|
17.为了确定三种可燃性气体:CH4、H2、CO(简称试验气),
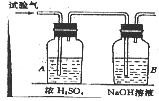 分别将它们在氧气中燃烧,把燃烧后生成的气体依次通过A、B两个
分别将它们在氧气中燃烧,把燃烧后生成的气体依次通过A、B两个
洗气瓶(如右图)。回答下列问题:
(1)装置A中的液体是 ;装置B中的液体是 。
(2)若装置A中的质量增加,B的质量不变,则试验气是 ,
燃烧的方程式为 。
(3)若装置A的质量不变,B的质量增加,则试验气是 ,B瓶中反应的化学方程式是 。
|