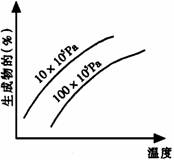
如果改变影响平衡的一个条件(如浓度、压强或温度),平衡就向着能够减弱这种改变的方向移动。具体见表6-1。
表6-1 外界条件对化学平衡的影响
|
改变影响平衡的一个条件 |
化学平衡移动方向 |
化学平衡移动结果 |
|
增大反应物浓度 |
向正反应方向移动 |
反应物浓度减小,但比原来大 |
|
减小反应物浓度 |
向逆反应方向移动 |
反应物浓度增大,但比原来小 |
|
增大生成物浓度 |
向逆反应方向移动 |
生成物浓度减小,但比原来大 |
|
减小生成物浓度 |
向正反应方向移动 |
生成物浓度增大,但比原来小 |
|
增大体系压强 |
向气体体积减小的反应方向移动 |
体系压强减小,但比原来大 |
|
减小体系压强 |
向气体体积增大的反应方向移动 |
体系压强增大,但比原来小 |
|
升高温度 |
向吸热反应方向移动 |
体系温度降低,但比原来高 |
|
降低温度 |
向放热反应方向移动 |
体系温度升高,但比原来低 |

 2NH3(g);△H=-Q
2NH3(g);△H=-Q