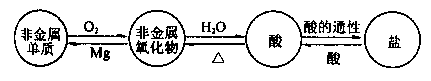(三)、金属的冶炼
1.金属冶炼主要是指将金属氧化物转化为金属的过程。在金属氧化物中加入还原剂,夺取金属氧化物中的氧,从而使其还原成全属单质。
2.可以作还原剂的物质主要有 碳 、 一氧化碳 和 氢气 。
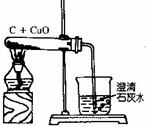
(1)、木炭和氧化铜粉末在高温下的反应:
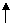 ∆
∆
C + 2CuO === 2Cu + CO2
实验现象:黑色固体逐渐变为红色,澄清石灰水变浑浊。
(2)、从孔雀石中冶炼铜:
①孔雀石(或铜锈)的主要成分为碱式碳酸铜,为绿色粉末。
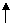 ∆
∆
②孔雀石加热: Cu2(OH)2CO3 === 2CuO + H2O + CO2
∆
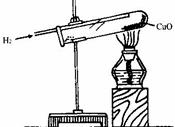
③氢气还原氧化铜: H2 + CuO === Cu + H2O
现象:黑色粉末状固体逐渐变为红色,试管口有水珠生成。
操作注意事项:实验开始时需先通一会氢气,再加热氧化铜,防止氢气与空气混合加热时试管爆裂;实验停止后,要继续通人氢气,直到试管冷却为止,防止灼热的铜被空气中的氧气氧化成氧化铜。
|
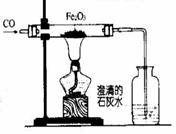
操作注意事项:实验最好在通风橱中进行。 实验时应该先通-会一氧化碳,以排除试管中的空气,防止一氧化碳与空气混合加热时引起爆炸。多余的一氧化碳不能直接排到空气中,应对着火焰烧掉。
3.含氧化合物里的氧被夺取的反应,叫做还原反应;能从氧化物中夺取氧的能力叫做还原性,具有还原性的物质可作还原剂。如碳、一氧化碳和氢气等。
重要提示:氢气还原氧化铜的实验装置中容易出现的典型错误:
(a)试管口高于试管底。应使试管口略低于试管底,防止反应生成的水倒流。
(b)试管口加了胶塞。 试管口不能加胶塞,否则气体排不出,容易造成试管炸裂。
(c)导管略伸入试管口。应使导管贴试管上壁伸入试管底部。
4.有关纯度问题的汁算
(1)根据混合物质量及其纯度,计算纯净物质量: 纯净物质量 = 混合物质量 × 纯度
(2)根据纯净物的质量,求出其中组成元素的质量分数。
组成元素的质量分数 = 某组成元素的质量 ÷ 纯净物的质量
(3)求工业产品中的含杂质的物质的质量(即混合物质量)
混合物质量 = 纯净物质量 ÷ 纯度
 (四)、
化合物之间的转化
(四)、
化合物之间的转化
1.鸡蛋外壳与稀盐酸的反应:CaCO3 + 2HCl ===CaCl2 + H2O + CO2
现象:一会下沉,一会又浮上来,不断地上下沉浮。
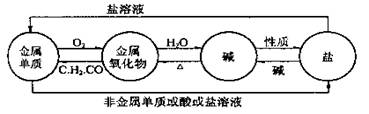
物质转化的规律
(1)金属 
 金属氧化物
金属氧化物 
 碱
碱 
 盐。如
盐。如
Ca 
 CaO
CaO
 Ca(OH)2
Ca(OH)2 
 CaCO3、
CaCO3、
(2)非金属 
 非金属氧化物
非金属氧化物 
 酸
酸 
 盐。如
盐。如
|
 CO2
CO2 
 H2CO3
H2CO3 
 Na2 CO3、
Na2 CO3、
(3)金属 + 非金属
 无氧酸盐。如2Na + Cl2 === 2NaCl
无氧酸盐。如2Na + Cl2 === 2NaCl
(4)金属氧化物 + 非金属氧化物 
 含氧酸盐。如Na2O + CO2
=== Na2CO3
含氧酸盐。如Na2O + CO2
=== Na2CO3
(5)酸 + 碱 
 盐 + 水。如HCl + NaOH === NaCl + H2O
盐 + 水。如HCl + NaOH === NaCl + H2O
 (6)盐 + 盐
(6)盐 + 盐 
 新盐 + 新盐。如NaCl + AgNO3 === AgCl + NaNO3
新盐 + 新盐。如NaCl + AgNO3 === AgCl + NaNO3
(7)金属氧化物 + 酸 
 盐 + 水。如Fe2O3 + 6HCl === 2FeCl3 + 3H2O
盐 + 水。如Fe2O3 + 6HCl === 2FeCl3 + 3H2O
(8)非金属氧化物 + 碱 
 盐 + 水。如SO2 + 2NaOH === Na2SO3 + H2O
盐 + 水。如SO2 + 2NaOH === Na2SO3 + H2O
 (9)金属 + 盐
(9)金属 + 盐 
 新全属 + 新盐。如Fe + CuSO4 === Cu + FeSO4
新全属 + 新盐。如Fe + CuSO4 === Cu + FeSO4
(10)金属 + 酸 
 盐 + 氢气。如Fe +2HCl === FeCl2 + H2
盐 + 氢气。如Fe +2HCl === FeCl2 + H2
1. 盐跟金属的反应,要求参加反应的盐必须是可溶的,由于盐跟金属的反应一般都在水溶液中进行,因此一些非常活泼能够跟水发生反应的金属(如钾、钙、钠等)也不符合要求。
2. 盐与盐的反应、盐与碱的反应除必须满足复分解反应的条件(生成物中有气体,水或沉淀)外,其反应物必须都可溶。