0 36334 36342 36348 36352 36358 36360 36364 36370 36372 36378 36384 36388 36390 36394 36400 36402 36408 36412 36414 36418 36420 36424 36426 36428 36429 36430 36432 36433 36434 36436 36438 36442 36444 36448 36450 36454 36460 36462 36468 36472 36474 36478 36484 36490 36492 36498 36502 36504 36510 36514 36520 36528 447348
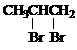 +2NaOH
+2NaOH
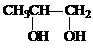 +2NaBr
+2NaBr 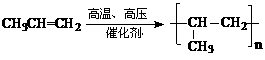
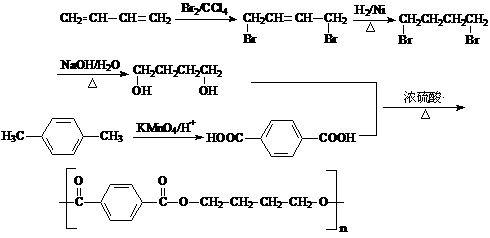
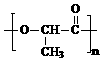
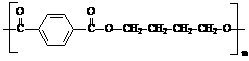 )是一种最重要的工程塑料之一。
)是一种最重要的工程塑料之一。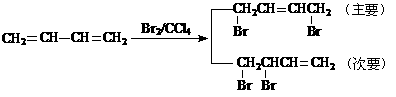
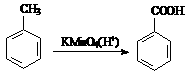
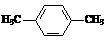 为原料合成PBT;请用反应流程图表示,并注明反应条件。
为原料合成PBT;请用反应流程图表示,并注明反应条件。 CH2=CH2
CH2=CH2
 CH2-CH2
CH2-CH2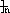
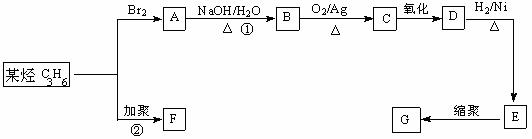
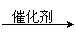 (3)X:加成反应;Y:消去反应;Z:加聚反应。
(3)X:加成反应;Y:消去反应;Z:加聚反应。 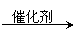 ②C H3CH2COOH
+ CH3OH
CH3CH2COOCH3 +H2O
②C H3CH2COOH
+ CH3OH
CH3CH2COOCH3 +H2O

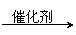 (4)写出下列转化的化学方程式:
(4)写出下列转化的化学方程式: