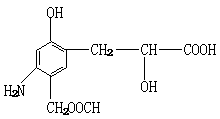
28.(8分)将固体FeC2O4·2H2O放在一个可以称出质量的容器里加热,固体质量随温度变化的有关典型数据如下表:
|
温度(℃) |
25 |
150 |
300 |
350 |
400 |
450 |
500 |
600 |
650 |
700 |
800 |
900 |
|
固体质量(g) |
1.0000 |
0.9022 |
0.8000 |
0.8000 |
0.4000 |
0.4020 |
0.4444 |
0.4444 |
0.4390 |
0.4300 |
0.4296 |
0.4296 |
据上述数据计算分析
a)300-350℃时质量不变的原因是什么?
b)350-400℃内发生反应的方程式__________________________
c)500℃时固体物质是什么?
d)600-800℃内发生反应的反应式__________________________
26.(15分)某无色溶液,其中有可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO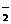 、S2-、CO
、S2-、CO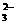 、SO
、SO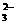 、SO
、SO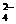 ,现取该溶液进行有关实验,实验结果如下图所示:
,现取该溶液进行有关实验,实验结果如下图所示:

 气体甲 气体乙
气体丙
气体甲 气体乙
气体丙
|
|||
|
|||
|


 无色溶液
溶液甲
溶液乙
溶渡丙
无色溶液
溶液甲
溶液乙
溶渡丙
 浅黄色沉淀甲
白色沉淀乙
白色沉淀丙
浅黄色沉淀甲
白色沉淀乙
白色沉淀丙
试回答下列问题:
(1)沉淀甲是____________,(2)沉淀乙是__________,由溶液甲生成沉淀乙的离子方程式为:_________________________________。(3)沉淀丙是__________。
(4)气体甲成分可能有哪几种?(可以不填满也可以补充,多填要扣分)
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
|
|
|
|
(5)综合上述信息,可以肯定存在的离子:____________________________________
23.(8分)以A、B两根石墨棒作电极,电解硝酸银溶液,通电10分钟时,在B极收集到气体11.2毫升(标况)然后将电源反接,以相同的电流强度再通电5分钟,此时与第一次通电前相比较,两极的质量变化分别是A极__________ B极________(填增大、减少、不变) 其数值分别是A_________ B__________ 若溶液的体积为200毫升(设体积不变)则溶液的pH值为___________。
|
①A+NaOH-→D+H2O ②B-→A+H2O ③C+NaOH(适量)-→B+NaCl
④E+H2O-→NaOH+F ⑤C+D+H2O-→B,则A、B、C、D化学式分别是:
A_____________ B_____________ C______________ D_____________
写出4摩C与6摩E在水溶液中发生反应的化学方程式:_______________________
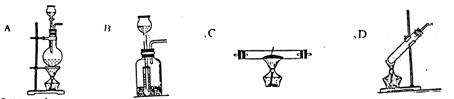 (16分)A-D是中学化学实验中常见的实验发生装置示意图
(16分)A-D是中学化学实验中常见的实验发生装置示意图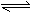 A.HB-水解方程式:HB-+H2O H3O++B2-
A.HB-水解方程式:HB-+H2O H3O++B2-