1. 钾是-种活泼的金属,工业上通常用金属钠和氯化钾在高温下反应制取。
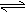 该反应为:Na(l)+KCl(l) NaCl(l)+K(g);ΔH >0
该反应为:Na(l)+KCl(l) NaCl(l)+K(g);ΔH >0
|
压强(kPa) |
13.33 |
53.32 |
101.3 |
|
K的沸点(℃) |
590 |
710 |
770 |
|
Na的沸点(℃) |
700 |
830 |
890 |
|
KCl的沸点(℃) |
|
|
1437 |
|
NaCl的沸点(℃) |
|
|
1465 |
该反应的平衡常数可表示为:K=[K],各物质的沸点与压强的关系见上表。
(1)在常压下金属钾转变为气态从反应混合物中分离的最低温度约为 ,而反应的最高温度应低 于 。
(2)在制取钾的过程中,为了提高原料的转化率可以采取的措施是____________________。
(3)常压下,当反应温度升高900℃时,该反应的平衡常数可表示为:K=______________
4. 在10℃和4×105Pa的条件下,当反应aA(g) dD(g) + eE(g)建立平衡后,维持温度不变,逐步增大体系的压强,在不同压强下该反应建立平衡后物质D的浓度见下表(在增大压强的过程中无其它副反应发生)
在10℃和4×105Pa的条件下,当反应aA(g) dD(g) + eE(g)建立平衡后,维持温度不变,逐步增大体系的压强,在不同压强下该反应建立平衡后物质D的浓度见下表(在增大压强的过程中无其它副反应发生)
|
压强(Pa) |
4×105 |
6×105 |
1×106 |
2×106 |
|
D的浓度( mol·L-1) |
0.085 |
0.126 |
0.200 |
0.440 |
(1) 压强从4×105Pa增加到6×105Pa时平衡应向______反应方向移动(正、逆),
理由是_____________________________;
(2) 压强从1×106Pa增加到2×106Pa时,平衡向______反应方向移动。此时平衡向该方向移动的两个必要条件是①______________________,②________________________。
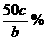 (3)(a + b -
(3)(a + b -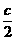 )mol (4)
)mol (4)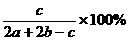 (5)a -c;b-
(5)a -c;b-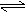
 在一定温度下,将n mol PCl5通入定容的密闭容器中,反应为:PCl5(g) PCl3(g)+ Cl2(g),达到平衡时测得压强为P1,若再向容器中通入n mol PCl5,又达平衡后,压强为P2,则下列关系式正确的是( )
在一定温度下,将n mol PCl5通入定容的密闭容器中,反应为:PCl5(g) PCl3(g)+ Cl2(g),达到平衡时测得压强为P1,若再向容器中通入n mol PCl5,又达平衡后,压强为P2,则下列关系式正确的是( )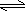 当反应Cl2+H2O HCl + HClO达到平衡后,欲使HClO的浓度增大,可以在氯水中加入( )
当反应Cl2+H2O HCl + HClO达到平衡后,欲使HClO的浓度增大,可以在氯水中加入( )