18.(6分)常温常压下,断裂1mol(理想)气体分子化学键所吸收的能量或形成1mol(理想)气体分子化学键所放出的能量称为键能(单位为KJ.mol-1)下表是一些键能数据(KJ·mol-1)
|
化学键 |
键能 |
化学键 |
键能 |
化学键 |
键能 |
化学键 |
键能 |
|
C-H |
414 |
C-F |
489 |
H-F |
565 |
F-F |
158 |
|
H-H |
436 |
H-N |
391 |
|
|
|
|
(1)根据键能数据计算以下反应的反应热△H:
CH4(g)+4F2(g)﹦CF4(g)+4HF(g) △H
(2)根据键能和反应热化学方程式 1/2N2(g)+3/2H2(g) = NH3(g ) △H = -46 kJ·mol-1 计算N≡N的键能。
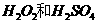 的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
的混合溶液可溶出印刷电路板金属粉末中的铜。已知: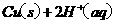 ====
====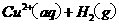
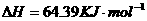
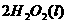 ====
====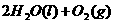
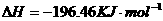
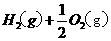 ====
==== 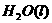
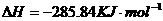
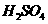 溶液中
溶液中 与
与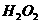 反应生成
反应生成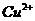 和
和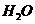 的热化学方程式为
的热化学方程式为 FeO(s)
FeO(s)  =-272.0KJ/mol
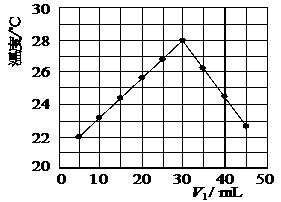
=-272.0KJ/mol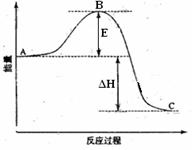 (13分)2SO2(g)+O2(g)
=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH = - 99kJ·mol-1。请回答下列问题:
(13分)2SO2(g)+O2(g)
=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH = - 99kJ·mol-1。请回答下列问题: 2NH3 ( g ) △H = -92.0
kJ/mol,将此温度下的1 mol N2 和3 mol H2 放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)
2NH3 ( g ) △H = -92.0
kJ/mol,将此温度下的1 mol N2 和3 mol H2 放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)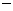 566 kJ/mol
566 kJ/mol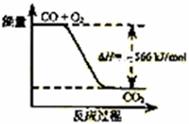 Na2O2(s)+CO2(g)=Na2CO3(s)+
Na2O2(s)+CO2(g)=Na2CO3(s)+
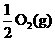 ΔH=
ΔH=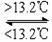 ③Sn(s,灰) Sn(s,白) ΔH3 = +2.1 kJ·mol-1
③Sn(s,灰) Sn(s,白) ΔH3 = +2.1 kJ·mol-1