22、(12分)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少N的氧化物在大气中的排放是环境保护的重要内容之一。
Ⅰ Ⅱ
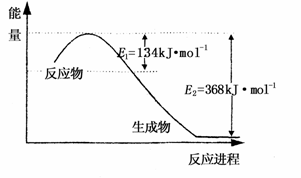
(1)图Ⅰ是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式 ;
又知:N2 (g) + O2 (g) = 2NO(g) △H= +180kJ·mol-1;
2NO(g) + O2(g) = 2NO2(g) △H= -112.3 kJ·mol-1;
则反应:2NO(g) + 2CO (g)  N2(g) + 2CO2 (g)的△H为
;
N2(g) + 2CO2 (g)的△H为
;
(2)一定温度下,在2L密闭容器中NO2和O2可发生下列反应:
4NO2(g)+O2 (g)  2 N2O5(g);已知体系中n(NO2)随时间变化如下表:
2 N2O5(g);已知体系中n(NO2)随时间变化如下表:
|
t(s) |
0 |
500 |
1000 |
1500 |
|
n(NO2)(mol) |
20 |
13.96 |
10.08 |
10.08 |
①写出该反应的平衡常数表达式:K= ,已知:K300℃>K350℃,则该反应
是 热反应
②反应达到平衡后,NO2的转化率为 ,此时若再通入一定量氮气,则NO2
的转化率将 (填“增大”、“减小”、“不变”);
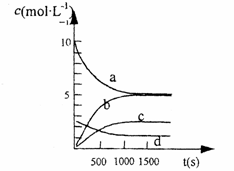
③图Ⅱ中表示N2O5 的浓度的变化曲线是 ,
用O2表示从0-500 s内该反应的平均速率v= 。
 0.2 NA
0.2 NA B.HClO的电子式:
B.HClO的电子式:
 D.某烷烃的名称为2-乙基丁烷
D.某烷烃的名称为2-乙基丁烷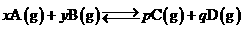
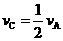 ;反应2min 时,A的浓度减少了
;反应2min 时,A的浓度减少了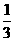 ,B的物质的量减少了
,B的物质的量减少了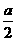 mol,有a mol D生成。
mol,有a mol D生成。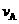 = ,
= ,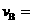 ;
;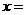 、
、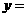 、
、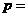 、
、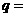 ;
; 0;(填“>”、“<”或“=”)
0;(填“>”、“<”或“=”)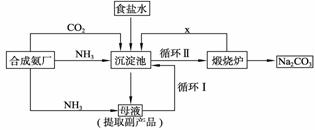
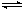 在一定温度下,反应1/2H2(g)+ 1/2X2(g) HX(g)的平衡常数为4。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于
在一定温度下,反应1/2H2(g)+ 1/2X2(g) HX(g)的平衡常数为4。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于