22. (10分)现用物质的量浓度为amol·L-1的标准NaOH溶液去滴定VmL盐酸的物质的量浓度,请填写下列空白:
(10分)现用物质的量浓度为amol·L-1的标准NaOH溶液去滴定VmL盐酸的物质的量浓度,请填写下列空白:
(1)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是________________________。
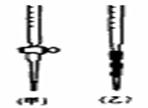
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入 (选填“甲”或“乙”)中。
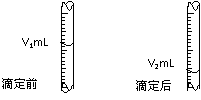 (3)右图是碱式滴定管中液面在滴定前后的读数, c(HCl)=_______________mol·L-1。
(3)右图是碱式滴定管中液面在滴定前后的读数, c(HCl)=_______________mol·L-1。
(4)若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定 管尖嘴部分气泡消失,则滴定的HCl物质的量浓度会偏____________(填“大”或“小”)。
(5)取20.00 mL待测盐酸放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用自己配制的标准液NaOH溶液进行滴定。重复上述滴定操作2-3次,记录数据如下。
|
实验编号 |
NaOH溶液的浓度(mol·L-1) |
滴定完成时, NaOH溶液滴入的体积(mL) |
待测盐酸的体积(mL) |
|
1 |
0.10 |
22.62 |
20.00 |
|
2 |
0.10 |
22.72 |
20.00 |
|
3 |
0.10 |
22.80 |
20.00 |
①滴定达到终点的标志是______________________________________________________。
②根据上述数据,可计算出该盐酸的浓度约为 (保留两位有效数字)。
19.(10分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
|
阳离子 |
H+、Na+、A13+、Ag+、Ba2+ |
|
阴离子 |
OH-、C1-、CO32-、NO3-、SO42- |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀。试回答下列问题:
(1)写出化学式:A___________________ D_________________________。
(2)写出A与E反应的离子方程式_____________________________________________。
(3)25℃时将40mL0.01mol·L-1B与20mL0.01mol·L-1C混合,最终溶液pH=____________。
(4)将C溶液逐滴加入等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为: 。
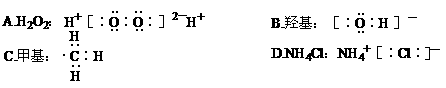
 是在普通锅的内侧涂覆上一层树脂而成,这层树脂的主要成分是聚四氟乙烯。洗衣店干洗西装是用有机溶剂来洗衣服的,目前使用的标准干洗剂的主要成分是四氯乙烯。关于聚四氟乙烯和四氯乙烯,下面的说法正确的是
是在普通锅的内侧涂覆上一层树脂而成,这层树脂的主要成分是聚四氟乙烯。洗衣店干洗西装是用有机溶剂来洗衣服的,目前使用的标准干洗剂的主要成分是四氯乙烯。关于聚四氟乙烯和四氯乙烯,下面的说法正确的是 A.它们都是乙烯的同系物
B.它们都属于混合物
A.它们都是乙烯的同系物
B.它们都属于混合物
 (6)工业上合成氨的反应是:N2(g)+3H2(g) 2NH3(g);△H=-92.2kJ·mol-1。
(6)工业上合成氨的反应是:N2(g)+3H2(g) 2NH3(g);△H=-92.2kJ·mol-1。