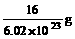3、仔细分析下列表格中烃的排列规律,判断排列在第12位的烃的分子式是( )
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
…… |
|
C2H2 |
C2H4 |
C2H6 |
C3H4 |
C3H6 |
C3H8 |
C4H6 |
C4H8 |
C4H10 |
…… |
A.C6H12 B.C6H14 C.C5H12 D.C5H10
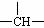 ,一个-Cl,它的可能的结构有 (
)
,一个-Cl,它的可能的结构有 (
)
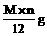 B、
B、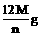
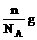 D、
D、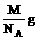
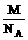 g。
g。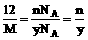 ,故y =
,故y =  NH3+H2O+CO2↑,则150℃时NH4HCO3分解产生的混合气体A的密度是相同条件下H2密度的 倍。
NH3+H2O+CO2↑,则150℃时NH4HCO3分解产生的混合气体A的密度是相同条件下H2密度的 倍。