16.(8分)“碘钟”实验中,3I-+S2O82--=I3-+2SO42-的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃、1个大气压条件下进行实验,得到的数据如下表:
|
实验编号 |
① |
② |
③ |
④ |
⑤ |
|
c(I-)/mol·L-1 |
0.040 |
0.080 |
0.080 |
0.160 |
0.120 |
|
c(S2O82-)/mol·L-1 |
0.040 |
0.040 |
0.080 |
0.020 |
0.040 |
|
t/s |
88.0 |
44.0 |
22.0 |
44.0 |
t1 |
回答下列问题:
(1)该实验的目的是 。
(2)显色时间t1= 。
(3)若在2个大气压下进行编号③对应浓度的实验,显色时间t2的范围为 (填序号)
A.<22.0s B.22.0s~44.0s C.>44.0s D.22.0s
(4)通过分析比较表中的数据,所得到的结论是 。
15.可逆反应:3A(g) 3B(?)+C(?);△H>0,随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是
( )
3B(?)+C(?);△H>0,随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是
( )
A.B和C可能都是固体 B.B和C一定都是气体
C.若C为固体,则B一定是气体 D.B和C不可能都是气体
第Ⅱ卷(55分)
|
9.工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)=Si(s)+4HCl(g);
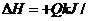 mol(Q>0) 某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是 ( )
mol(Q>0) 某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是 ( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ
C.反应至4
min时,若HCl浓度为0.12
mol/L,则H2的反应速率为0.03 mol/(L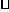 min)
min)
D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol/LNaOH溶液恰好反
应
|
A.判断反应的方向 B.确定反应是否一定发生
C.判断反应过程发生的速率 D.判断反应过程的热效率
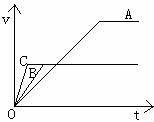 (6分)右图中A、B、C三条曲线分别表示足量的Na2CO3和
(6分)右图中A、B、C三条曲线分别表示足量的Na2CO3和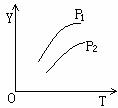 如下图所示,不同温度和压强下,在容积不变的密闭容器中对可逆反应:4L(g)
如下图所示,不同温度和压强下,在容积不变的密闭容器中对可逆反应:4L(g)
 CO2 + H2
CO2 + H2  2C(g)
2C(g) <0达到平衡后,将气体混合物的温度降低,下列叙述中正确的是
( )
<0达到平衡后,将气体混合物的温度降低,下列叙述中正确的是
( )