17 (共15分)
A、(8分)用双线桥表示下列反应中得失电子的情况,该反应的氧化剂 、
氧化产物 、该反应中被还原的HNO3与未被还原的HNO3的质量
之比为 。
3FeO + 10HNO3 == 3Fe(NO3)3 + NO↑ + 5H2O.
B、(3分)配平:
SO32- + MnO4- + H+ - Mn2+ + SO42- + H2O
C、(4分)在一定条件下,可逆反应:mA+nB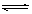 pC达到平衡,若:
pC达到平衡,若:
(1)A、B、C都是气体,减少压强,平衡向正反应方向移动,则m+n和p的
关系是 ;
(2)A、C是气体,增加B的量,平衡不移动,则B为 态;
(3)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的
方向是 ;
(4)加热后,可使C的质量增加,则正反应是 反应(放热或吸热)。
18.(6分)在某一容积为VL的密闭容器内,加入等物质的量的X和Y,在一定的条件下发生
如下反应:X(g)+Y(g)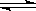 2Z (g)。(正反应是放热反应)
2Z (g)。(正反应是放热反应)
(1)反应达到平衡后,若降低温度,化学反应速率 ,Z的浓度 。
(填“增大”、“减小”或“不变”)。
(2)图1、图2表示该反应在t1时达到平衡、在t2时因改变某个条件而发生变化的曲线:
|
|
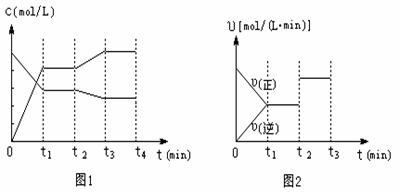
由图1判断,反应进行至t2 min时,曲线发生变化的原因是
。(用文字表达)。
由图2判断,t2 min到t3 min 的曲线变化的原因可能是 (填编号)
a.降低温度 b.加了催化剂 c.增加Z的量 d.缩小容器体积

 氧化铜
氧化铜 蒸发结晶
蒸发结晶
 4Z(g)+W(s)反应,达
4Z(g)+W(s)反应,达