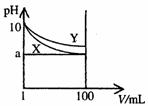
22.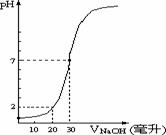 下图为10mL一定物质的量浓度的盐酸X,用一定物质量浓度的NaOH溶液Y滴定的图示,据图推出NaOH溶液和盐酸的物质量的浓度正确的是( )
下图为10mL一定物质的量浓度的盐酸X,用一定物质量浓度的NaOH溶液Y滴定的图示,据图推出NaOH溶液和盐酸的物质量的浓度正确的是( )
|
|
A |
B |
C |
D |
|
[HCl](mol/L) |
0.12 |
0.04 |
0.12 |
0.09 |
|
[NaOH](mol/L) |
0.04 |
0.12 |
0.06 |
0.03 |
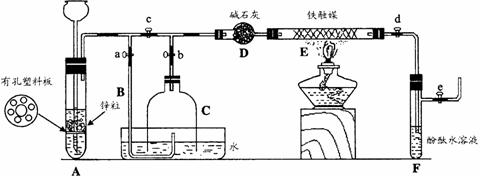
 cC(s)+dD(g);△H=a kJ/mol在该反应中,a=b=c=d=1,当反应经过5min后达到平衡状态,此时测得混合气体的总物质的最为0.34mol。请回答下列问题:
cC(s)+dD(g);△H=a kJ/mol在该反应中,a=b=c=d=1,当反应经过5min后达到平衡状态,此时测得混合气体的总物质的最为0.34mol。请回答下列问题: 2C(g) + D(g)
2C(g) + D(g)