22.(12分)某校化学小组学生进行如下实验。
(1)使用铜和稀硫酸制备硫酸铜晶体。
步骤如下
|
|
|
|
|||||||
|
|||||||
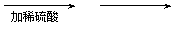 |
|||||||
 |
|||||||
步骤①观察到的现象是 。
步骤③的主要操作包括: 。
(2)硫酸铜溶解度的测定。
 用石墨电极(相同)电解饱和CuSO4溶液,阴极的电极反应式
用石墨电极(相同)电解饱和CuSO4溶液,阴极的电极反应式
是 。已知饱和CuSO4溶液的质量为60 g,通电10 min后,溶液恰好变为无色。称量发现两电极质量差为4 g,此温度下CuSO4的溶解度是 ___ 。
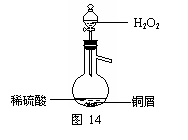
(3)某同学查询资料得知:铜屑放入稀硫酸中不发生反应,若在稀硫酸中加入H2O2,铜屑可逐渐溶解。实验小组同学设计实验装置如右图,验证该实验,该反应的化学方程式
是 。
若将H2O2和稀硫酸加入烧瓶中的顺序颠倒,实验得
到的结论是
。
草 稿 纸
21.(18分)现有烯烃A可合成饱和酯G:
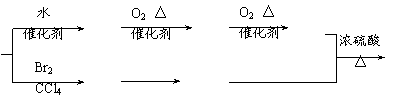
B C D
|
E F
(1)、A、G的结构简式分别是:A__________________G、____________________。
(2)、写出下列反应方程式,并注明反应类型
 ①、E
F:
①、E
F:
___________________________________________ ______________
 ②、D
+ F G
:
②、D
+ F G
:
___________________________________________ ______________
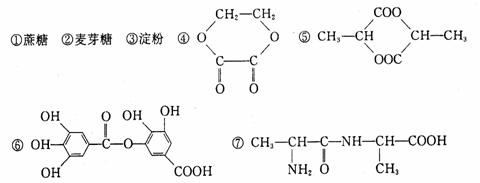
(3)、写出与D的通式相同,碳原子个数是D的两倍,属于酯类的所有同分异构体的结构简式
_____________、______________、____________、_______________。
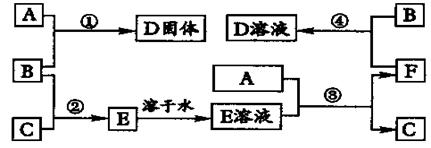

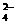 +4H+
+4H+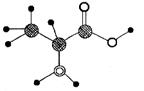 下图是某有机物分子的简易球棍模型,该有机物中只含C、H、O、N四种元素。下列关于该有机物的说法中错误的是( )
下图是某有机物分子的简易球棍模型,该有机物中只含C、H、O、N四种元素。下列关于该有机物的说法中错误的是( )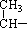 CH2-CH2-
CH2-CH2-