0 24232 24240 24246 24250 24256 24258 24262 24268 24270 24276 24282 24286 24288 24292 24298 24300 24306 24310 24312 24316 24318 24322 24324 24326 24327 24328 24330 24331 24332 24334 24336 24340 24342 24346 24348 24352 24358 24360 24366 24370 24372 24376 24382 24388 24390 24396 24400 24402 24408 24412 24418 24426 447348
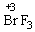 →
→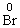 得电子3e-×1 mol=3 mol e-,根据电子守恒则由水还原的BrF3的物质的量为
得电子3e-×1 mol=3 mol e-,根据电子守恒则由水还原的BrF3的物质的量为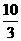 mol。
mol。 (2)从KOCN+KOH+Cl2→CO2+N2+KCl+H2O可知,N元素的化合价从-3升至0,而Cl元素的化合价从0降至-1,根据氧化还原反应中元素化合价升降数相等的规律,即可配得:
(2)从KOCN+KOH+Cl2→CO2+N2+KCl+H2O可知,N元素的化合价从-3升至0,而Cl元素的化合价从0降至-1,根据氧化还原反应中元素化合价升降数相等的规律,即可配得:
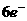
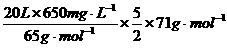 =35.5g
=35.5g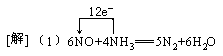

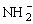 +H+,H-与NH3分子的反应实质上就是H-和NH3分子电离出来的H+发生反应生成H2,由于H-失电子能力强,所以H-是很强的还原剂。NH3分子中的H得到电子,它是氧化剂。H2是H-失电子的氧化产物,也是H+得电子的还原产物,因此H2既是氧化产物又是还原产物。由于该反应中无单质参加,该反应不符合置换反应的定义。
+H+,H-与NH3分子的反应实质上就是H-和NH3分子电离出来的H+发生反应生成H2,由于H-失电子能力强,所以H-是很强的还原剂。NH3分子中的H得到电子,它是氧化剂。H2是H-失电子的氧化产物,也是H+得电子的还原产物,因此H2既是氧化产物又是还原产物。由于该反应中无单质参加,该反应不符合置换反应的定义。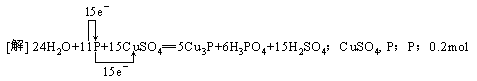
 2FeCl3
2FeCl3