38.元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表是元素周期表的一部分,请依据该表回答问题。
|
族 周期 |
IA |
|
0 |
|||||
|
1 |
H |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
He |
|
2 |
Li |
Be |
B |
C |
N |
O |
F |
Ne |
|
3 |
Na |
Mg |
Al |
Si |
P |
S |
Cl |
Ar |
(1)可用于半导体材料的元素是 (填元素符号),它在元素周期表中的位置为 。
(2)第3周期IA族元素的原子结构示意图是 ,该元素与同周期VIIA族元素组成的化合物类型是 。该化合物在生产生活中有广泛用途,请举一例 。
(3)第3周期元素的最高价氧化物对应水化物中,酸性最强的是 (填化学式,下同);碱性最强的是 ;具有两性的是 ,其与氢氧化钠溶液反应的化学方程式为 。
(4)由H、N、O三种元素组成的离子化合物X,在 210℃时可分解生成N元素的一种气态氧化物Y和水。已知 40 g X完全分解可生成11.2 L(标准状况)Y,则Y的化学式为 。
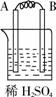
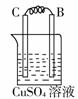
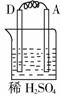
36.由A、B、C、D四种金属按下表中装置进行实验,根据实验现象填表:
|
装 置 |
 |
 |
 |
|
现
象 |
金属A不断溶解 |
C的质量增加 |
A上有气体产生 |
|
正极反应式 |
|
|
|
|
四种金属活动性由强→弱的顺序 |
|
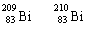 铋(Bi)在医药方面有重要应用。 下列关于 和 的说法正确的是( )
铋(Bi)在医药方面有重要应用。 下列关于 和 的说法正确的是( )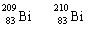
 B. 和 互为同位素
B. 和 互为同位素 别含有126和127个质子
别含有126和127个质子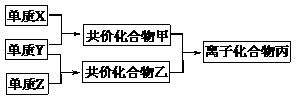
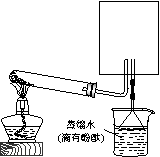 (1)X的电子式是
。
(1)X的电子式是
。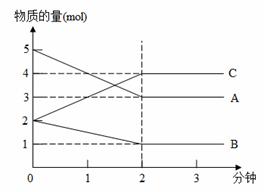 某可逆反应从0-2 分钟进行过程中,在不同反应时间各物质的量变化情况如图所示。则该反应的反应物是____,生成物是_____,化学方程式为_______;
某可逆反应从0-2 分钟进行过程中,在不同反应时间各物质的量变化情况如图所示。则该反应的反应物是____,生成物是_____,化学方程式为_______;