0 22730 22738 22744 22748 22754 22756 22760 22766 22768 22774 22780 22784 22786 22790 22796 22798 22804 22808 22810 22814 22816 22820 22822 22824 22825 22826 22828 22829 22830 22832 22834 22838 22840 22844 22846 22850 22856 22858 22864 22868 22870 22874 22880 22886 22888 22894 22898 22900 22906 22910 22916 22924 447348
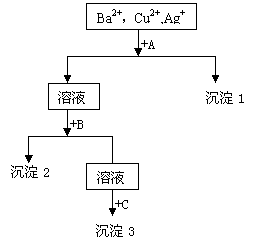 5(7分).某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如右
5(7分).某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如右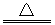 KClO3+5KCl+3H2O中,氧化剂与还原剂物质的量之比为( )
KClO3+5KCl+3H2O中,氧化剂与还原剂物质的量之比为( )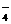 →Mn2+如果分别用等物质的量的这些物质氧化足量的FeCl2溶液,得到Fe3+最多的是 ( )
→Mn2+如果分别用等物质的量的这些物质氧化足量的FeCl2溶液,得到Fe3+最多的是 ( )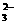 +2H+
+2H+ CO2↑+H2O ②Ba2++2OH-+2H++SO
CO2↑+H2O ②Ba2++2OH-+2H++SO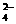
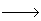 NaCl+NH4NO2
第二步:NH4NO2
NaCl+NH4NO2
第二步:NH4NO2 N2↑+2H2O
N2↑+2H2O