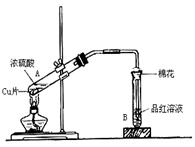
17、某同学用如图装置进行铜与一定体积已知浓度的浓硫酸反应的实验研究。
(1)写出A、B两试管中的实验现象:
A________ _____、 (两种即可);B 。
(2)充分反应后,发现铜和硫酸都有剩余。在不补充浓硫酸的前提下,若使剩余铜片溶解,可再加入物质的化学式为___ _。
(3)测定剩余硫酸的物质的量时,先测铜与浓硫酸反应产生SO2的量,再计算余酸的物质的量。他认为测定SO2的量的方法有多种,下列方案中不可行的是( )
A.将A产生的气体干燥后缓缓通过预先称量的盛有碱石灰的干
燥管,结束反应后再次称量
B.将A产生的气体缓缓通入稀硫酸酸化的KMnO4溶液,加足
量BaCl2溶液,过滤、洗涤、干燥、称量沉淀
C.将A产生的气体缓缓通入足量用HNO3酸化Ba(NO3)2溶液,充分反应过滤、洗涤、干燥、称量沉淀
D.用排饱和NaHSO3溶液的方法测出干燥后装置A产生SO2气体的体积(已折算成标准状况)
(4)向反应后的溶液中加入足量的氧化铜,使剩余的硫酸转化为硫酸铜,过滤后将滤液加热浓缩,冷却制得硫酸铜晶体(CuSO4·xH2O),用加热法测定该晶体里结晶水x的值。其中一次实验的数据为:
|
坩埚质量 |
坩埚与晶体总质量 |
加热后坩埚与固体总质量 |
|
11.7g |
22.7g |
18.6g |
根据数据计算,判断x '的实测值比理论值(x=5)_________(填“偏大”或“偏小”),实验中产生误差的原因可能是_________(填字母编号):
A. 硫酸铜晶体中含有不挥发杂质
B.加热失水后露置在空气中冷却
C.加热时有晶体飞溅出去
D.硫酸铜晶体(CuSO4·xH2O)在称量前晶体的表面吸收了水份
 与S粉反应时,有一部分与O2生成Na2O2,已知所得混合物中O的质量分数为13.67%,且混合物中有Na2S和Na2
O2,则混合物中硫的质量分数为( )
与S粉反应时,有一部分与O2生成Na2O2,已知所得混合物中O的质量分数为13.67%,且混合物中有Na2S和Na2
O2,则混合物中硫的质量分数为( ) ”(读音为伦)。下列说法正确的是( )
”(读音为伦)。下列说法正确的是( ) 右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。
右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。